STUDIO NATALEE. RIBOCICLIB ADIUVANTE NEL CARCINOMA MAMMARIO.
A – Durante il congresso tenutosi a Chicago a giugno 2023, sono stati presentati i risultati dello studio NATALEE
Ribociclib and endocrine therapy as adjuvant treatment in patients with HR+/HER2- early breast cancer: primary results from the Phase III NATALEE trial. SLAMON D et al. J Clin Oncol. 2023;41_suppl 17:LBA500

Circa l’80% dei nuovi casi di carcinoma mammario sono forme non metastatiche (Early Breast Cancer-EBC) e di queste circa il 70-75%, sono rappresentati da carcinomi HR+/HER2-negativi. Il 32% dei pazienti con HR+/HER2-negativi hanno uno STADIO II di malattia, mentre più bassa è la percentuale dei pazienti STADIO III. L’obiettivo del trattamento dell’EBC (chirurgia ± radioterapia adiuvante, endocrinoterapia adiuvante± chemioterapia) è la guarigione del paziente. Tuttavia, anche dopo aver ricevuto una terapia endocrina adiuvante, il 27-37% dei pazienti STADIO II e oltre il 50% dei pazienti stadio III presenta una ripresa a distanza di malattia a 20 anni dalla diagnosi (PAN H. et al. NEJM 2017; 377: 1836-1846).
In considerazione dei risultati ottenuti con ribociclib nelle forme avanzate di carcinoma mammario, è stato disegnato lo studio clinico NATALEE.
Poiché una durata prolungata del trattamento è fondamentale per prolungare l’arresto del ciclo cellulare e portare un maggior numero di cellule tumorali alla senescenza o alla morte, è stata scelta una durata di 3 anni del trattamento con Ribociclib alla dose di 400 mg per migliorare la tollerabilità e mantenere l’efficacia.
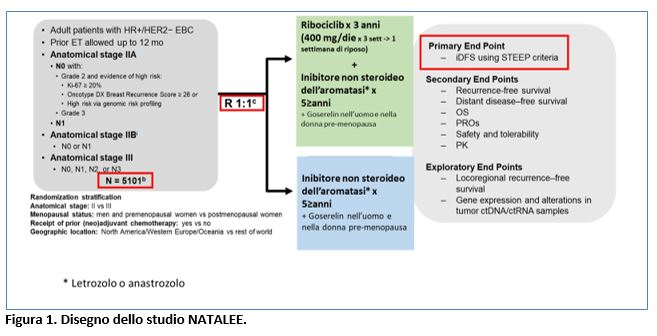
Lo studio NATALEE è uno studio di fase 3 randomizzato che ha arruolato 5.101 pazienti (uomini e donne pre/post-menopausa) in stadio patologico II e III con carcinoma mammario HR+/HER2-negativo in fase precoce.
I pazienti sono stati randomizzati (1:1) a ricevere ribociclib (400 mg/os /die per 3 settimane àuna settimana di sospensione) associato a inibitore non steroideo dell’aromatasi (letrozolo o anastrozolo) oppure solo ormonoterapia adiuvante. Gli uomini e le donne in pre-menopausa ricevevano anche Goserelin (3,6 gr/IM ogni 28 giorni). Il RIBOCICLIB veniva somministrato per 3 anni e dell’aromatasi per ≥ 5 anni.
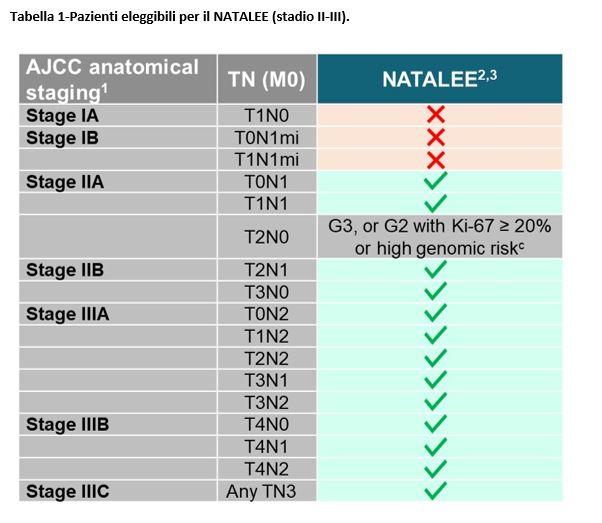
L’endpoint primario dello studio era l’invasive-DFS. Nella tabella 1 sono ripotati i criteri di eleggibilità.
Nello studio NATALEE sono stati arruolati 20 uomini (0,4%). Circa il 44% delle donne arruolate erano in pre-menopausa e il 56% in post-menopausa. Il 20% dei pazienti era in stadio patologico II A, il 20% II B e il 60% III. Il 41% dei pazienti aveva ricevuto chemioterapia in (neo)-adiuvante. Ad un follow up mediano di 27,7 mesi (quando solo il 20% dei pazienti aveva completato i 3 anni di ribociclib), è stata effettuata la 2° interim analysis con 426 eventi per la iDFS, che ha riportato un vantaggio statisticamente significativo nel gruppo ribociclib rispetto al gruppo di controllo (3y iDFS: 90,4% vs 87,1%) con un beneficio assoluto a 3 anni del 3,3%. Il rischio di malattia invasiva è stato ridotto del 25,2% dall’aggiunta del ribociclib all’ormonoterapia adiuvante con HR=0,748 ( 95% CI 0,618-0,906; p= 0.0014). Il beneficio in iDFS è risultato consistente in tutti i sottogruppi di pazienti pre-specificati. Anche per l’endpoint secondario distant-DFS (DDFS) è stato evidenziato un vantaggio statisticamente significativo con l’aggiunta di ribociclib, con una DDFS a 3 anni pari al 90,8% vs 88,6% (HR 0,739; 95% CI 0,603-0,905;p=0.0017) e con un beneficio assoluto a 3 anni del 2,2%.
Ad un follow up mediano di 30,4 mesi sono stati registrati 61 eventi (decessi) per il braccio Ribociclib vs 73 eventi per il braccio di controllo e l’overall survival (OS) non è significativa, ma i dati per la OS non sono ancora maturi.
La dose iniziale di Ribociclib di 400 mgr è stata ben tollerata. L’evento collaterale più frequente correlato a ribociclib è stato la neutropenia (qualsiasi grado: 62% vs 4,5%; di grado ≥63: 43,8% vs 0,8%), con solo lo 0,3% di neutropenia febbrile. Gli effetti collaterali più frequenti che hanno portato a interruzione della terapia sono stati gli eventi avversi epatici (8,9% per Ribociclib vs 0,1% per braccio della sola endocrinoterapia). Relativamente agli eventi cardiaci e polmonari, sono stati registrati prolungamenti del QT di qualsiasi grado con ribociclib nel 4,2% dei pazienti (percentuale inferiore al 6,5% riportata nello studio MONALEESA con 600 mgr di ribociclib) e di grado 3 solo nello 0,2% ( rispetto all’1,2% riportato nello studio MONALEESA). La polmonite interstiziale è stata riportata nell’1,5% dei pazienti del gruppo ribociclib, senza nessun caso di grado 3-4.
B – All’ ESMO (20-24 ottobre 2023) sono stati presentati i risultati di una analisi esploratoria pre-specificata di sottogruppo.
Invasive disease-free survival (iDFS) cross key subgroups from the Phase III NATALEE study of ribociclib (RIB) + a nonsteroidal aromataser inhibitor (NSAI) in patients (pts) with HR+/HER2- early breast cancer (EBC). Bardia A et al, ESMO CONGRESS 2023, LBA23

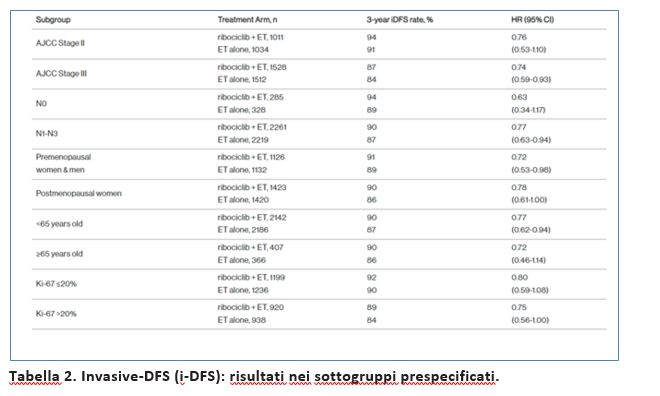
Nell’analisi di sottogruppo prespecificata dello studio NATALEE dell’invasive-DFS (iDFS), a 27,7 mesi di follow up viene evidenziato un beneficio in iDFS con ribociclib+ ormonoterapia adiuvante in tutti i sottogruppi prespecificati rispetto alla sola ormonoterapia adiuvante nei pazienti con stadio II e III HR+/HER2- EBC, inclusi i pazienti pN0 e stadio II e i pazienti ultr65enni (Tabella 2).
C – Al San Antonio Breast Cancer Symposium (SABCS), 5-9 dicembre 2023, è stata presentata l’analisi finale dell’i-DFS.
Ribociclib +Nonsteroidal aromatase inhibitor as adjuvant treatment in patients with HR+/HER2- early breast cancer: final invasive disease-free survival analysis from the NATALEE trial. Hortobagyi G.N. et al. Abstract GS03-03, SABCS 2023.

Alla data del cutoff per l’analisi finale dell’iDFS ( 21 luglio 2023), presentata a SABCS 2023, si erano verificati 509 eventi totali.
Delle 2.549 pazienti arruolate nel gruppo ribociclib+NSAI, 1.996 (78,3%) avevano terminato l’assunzione di ribociclib: il 42,8% (1.091) delle pazienti perché avevano completato i tre anni di assunzione previsti (rispetto al 20,2% della seconda interim analisi i cui dati erano stati presentati all’ASCO 2023) e 905 (35,5%) perché avevano interrotto l’assunzione prima dei tre anni previsti. Il tasso di pazienti che ha interrotto il ribociclib per eventi avversi è rimasto stabile rispetto all’analisi presentata all’ASCO 2023 (19,5% vs 18,7% dell’analisi precedente). Il 20,7% (528) delle pazienti stava ancora assumendo ribociclib rispetto al 45% della analisi precedente (ASCO 2023).
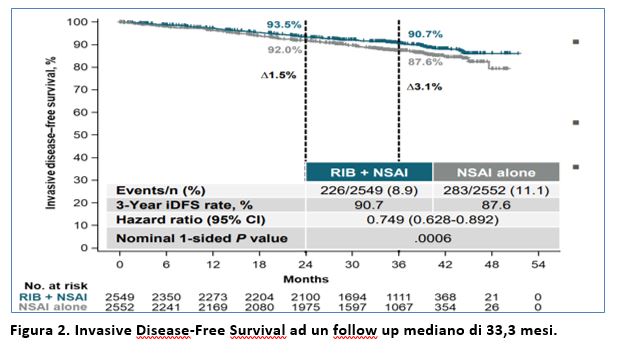
Il follow up mediano era di 33,3 mesi (5,6 mesi in più rispetto alla seconda interim analisi presentata all’ASCO 2023). Il tasso di iDFS a 3 anni è stato pari al 90,7% per il gruppo ribociclib+NSAI vs 87,6% per il gruppo solo NSAI, con un beneficio assoluto a 3 anni del 3,1% (HR=0,749; 95%CI 0,628-0,892; p=0,0006) (Figura 2).
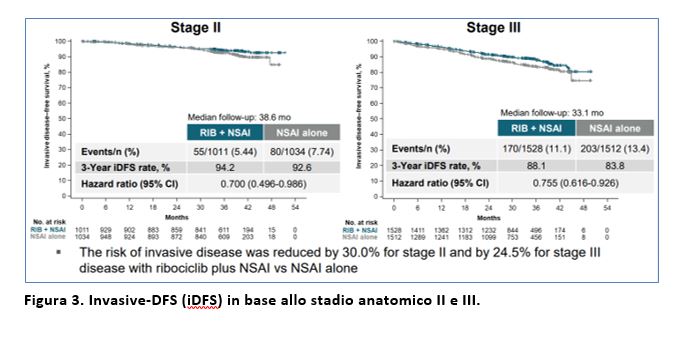
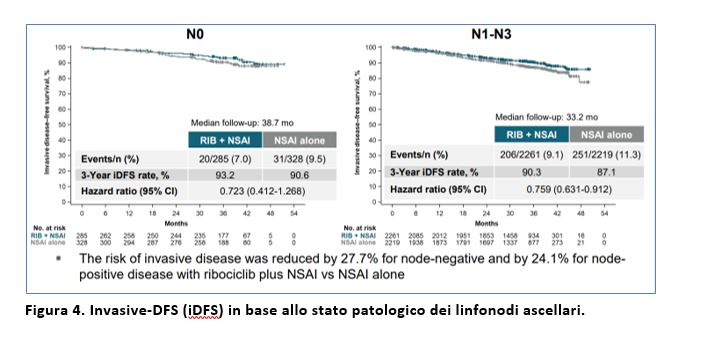
Il beneficio in iDFS con l’aggiunta del ribociclib all’endocrinoterapia è stato consistente nei sottogruppi prespecificati, compresi i pazienti con stadio II, stadio III, linfonodi ascellari negativi e positivi (Figura 3 e 4).
Il beneficio assoluto in distant-DFS (endpoint secondario) con ribociclcib è stato pari al 2,7% a 3 anni (92,9% vs 90,2%; HR=0,749; 95% CI 0,623-0,900; p=0,0010). Relativamente alla Overall Survival (endpoint secondario), ad un follow up mediano di 35,9 mesi sono stati registrati meno del 4% di eventi (decessi) in entrambi i gruppi di pazienti e sarà quindi necessario un follow up più lungo (OS a 3 anni: 97% vs 96,1%; HR=0,892; 95% CI 0,661-1,203).
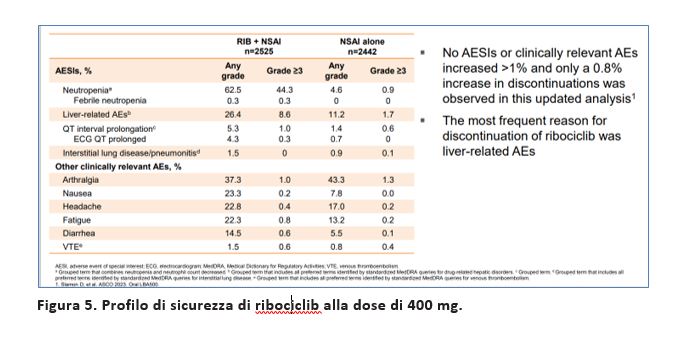
L’incidenza dei più frequenti eventi avversi osservati è risultata stabile anche ad un follow up più lungo, con un regime di ribociclib di 3 anni (a una dose iniziale di 400 g) che è risultato ben tollerato nel setting adiuvante (Figura 5).
COMMENTO
L’aggiunta di ribociclib (alla dose iniziale di 400 mg) all’endocrinoterapia adiuvante con letrozolo o anastrozolo ha evidenziato, nello studio di fase 3 NATALEE, un vantaggio statisticamente significativo e clinicamente rilevante nelle pazienti con EBC HR+/HER2-negativo in invasive-DFS a 3 anni (endpoint primario) con un beneficio assoluto pari al 3,1% in tutta la popolazione.
Il beneficio in iDFS con ribociclib è stato consistente nei sottogruppi prespecificati, e in particolare anche nei pazienti stadio patologico II, stadio patologico III, linfonodi ascellari negativi e linfonodi ascellari positivi.
Anche per l’endpoint secondario distant-DFS, è stato evidenziato un vantaggio statisticamente significativo con l’aggiunta di ribociclib, con un beneficio assoluto a 3 anni del 2,7%.
Ribociclib per 3 anni alla dose iniziale di 400 mg è risultato inoltre ben tollerato.
Per la Overall Survival (altro endpoint secondario) i dati sono ancora immaturi.