
PHASE II EFFICACY AND SAFETY OF 80 MG OSIMERTINIB WITH LEPTOMENINGEAL METASTASES ASSOCIATED WITH EPIDERMAL GROWTH FACTOR RECEPTOR MUTATION-POSITIVE NON-SMALL CELL LUNG CANCER (BLOSSOM).
Park S, Baldry R, Jung HA, Sun JM, Lee SH, Ahn JS, Kim YJ, Lee Y, Kim DW, Kim SW, Lee KH, Lee WJ, Choi JW, Chong K, Lee JI, Gwon SH, Son NH, Ahn MJ.
J Clin Oncol. 2024 Aug 10;42(23):2747-2756. doi: 10.1200/JCO.24.00708
Link all’abstract
https://pubmed.ncbi.nlm.nih.gov/38828959/
L’incidenza di metastasi leptomeningee (LM) è più elevata nei pazienti con NSCLC e mutazioni di EGFR rispetto ai pazienti WILD-TYPE : 9,4% vs 1,7% in una analisi retrospettiva di 5.387 casi (Li Y-S et al, J.Thorac Oncol 2016).
La sopravvivenza globale mediana dei pazienti con LM varia da 3 a 10 mesi vista anche la limitata efficacia dei trattamenti convenzionali come la chemioterapia intratecale o la radioterapia panencefalica (WBRT).
In considerazione delle elevate capacità di OSIMERTINIB (un inibitore di TK-EGFR di terza generazione) di penetrazione attraverso la barriera emato-encefalica e dei dati retrospettivi di PFS e OS riportati in pazienti con metastasi alle leptomeningi, è stato condotto uno studio prospettico per valutare l’efficacia e la safety di 80 mg/dei di OSIMERTINIB in pazienti con NSCLC e mutazione EGFR che hanno sviluppato malattia leptomeningea dopo trattamento con inibitori della TK-EGFR di prima/seconda generazione.
METODI
In questo studio multicentrico di fase II, open-label, single-arm, condotto in sei ospedali della Repubblica della Corea, è stato somministrato OSIMERTINIB (80 mg/die) a pazienti con NSCLC e mutazione EGFR che avevano sviluppato metastasi alle leptomeningi dopo terapia con TKI-EGFR.
L’endpoint primario dello studio era la sopravvivenza globale (OS).
Endpoint secondari includevano:
- Tasso di risposte obiettive a livello delle leptomeningi (LM-ORR);
- Durata della risposta (DOR);
- Tasso di controllo di malattia (DCR);
- PFS analizzata da una commissione esterna indipendente ( BIRC= Blinded Indipendent Central Review) neuroradiologica che ha valutato la risposta delle metastasi leptomeningee in base ai criteri RANO-LM- (Chamberlain M, Neuro Oncol 2017).
Gli investigatori hanno valutato ORR, DOR e le risposte nelle leptomeningi, parenchima cerebrale e lesioni extracraniche secondo RECIST v.1 (Eisenhauer E.A., Eur. J. Cancer 2009).
Sono stati valutati anche: la qualità della vita (QLQ-C30 e QLQ-BN20); i profili di (CTCAE v.5.0); la citologia del liquido cefalo-rachidiano (CSF) al basale, dopo 3 cicli e al momento della progressione di malattia; le concentrazioni di osimertinib nel plasma e nel CFS (al 1° giorno del ciclo 3 e del ciclo 6).
RISULTATI
Nello studio BLOSSOM sono stati arruolati 73 pazienti, dei quali 64 valutabili a livello leptomeningea dalla commissione indipendente radiologica. Dei 64 pazienti (65,7% donne) 62 (97,3%) erano T790M-negativi e 2 (2,7%) T790M-positivi.
Precedenti trattamenti per metastasi leptomeningee includevano:
- Radioterapia panencefalica: 13,7% ;
- Methotrexate intratecale: 12,3% ;
- Inserzione di Ommaya: 20,6% ;
- Shunt ventricolo-peritoneale: 6,9% .
La citologia del liquor era positiva nell’84,7% dei 46 pazienti testati.
Ad un follow up mediano di 15,6 mesi (95% CI : 11,5-20,2), la PFS intracranica mediana era, nei 73 pazienti arruolati, di 12,5 mesi e la sopravvivenza globale di 15,6 mesi (Figura 1).
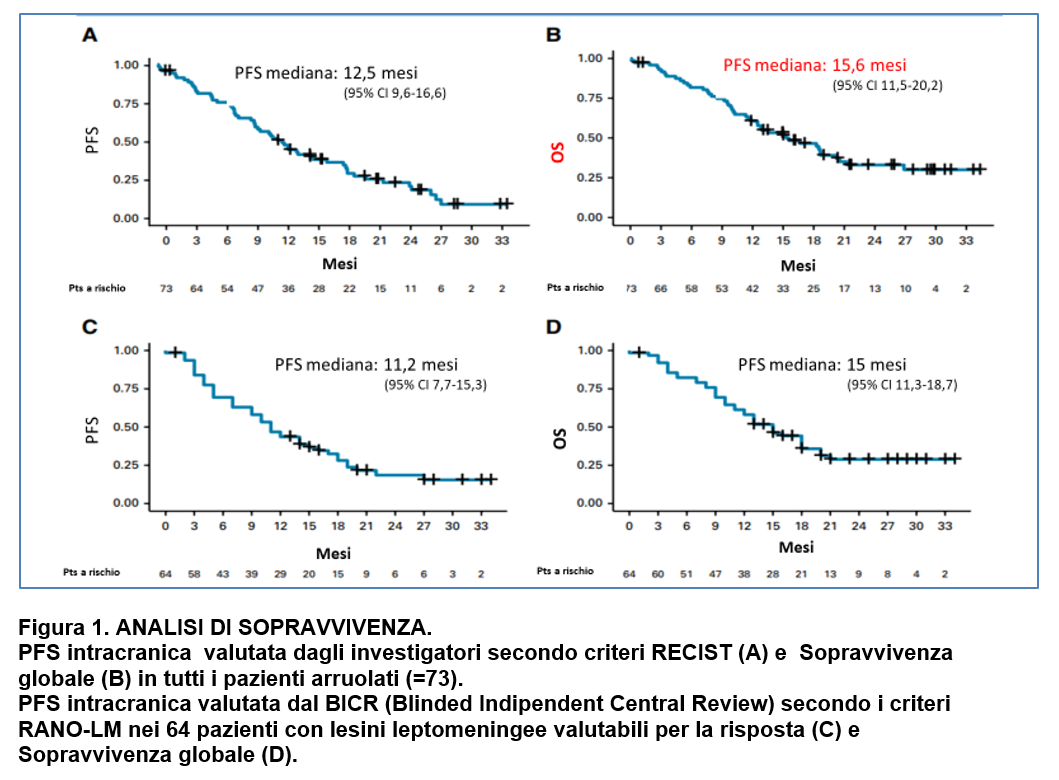
Dei 64 pazienti valutabili per la risposta LM, alla data dell’analisi (25 ottobre 2023) il 75% era deceduto o presentava progressione.
In accordo alla valutazione della risposta degli investigatori secondo i criteri RECIST, la PFS mediana intracranica era 12,5 mesi e la DOR di 20,3 mesi.
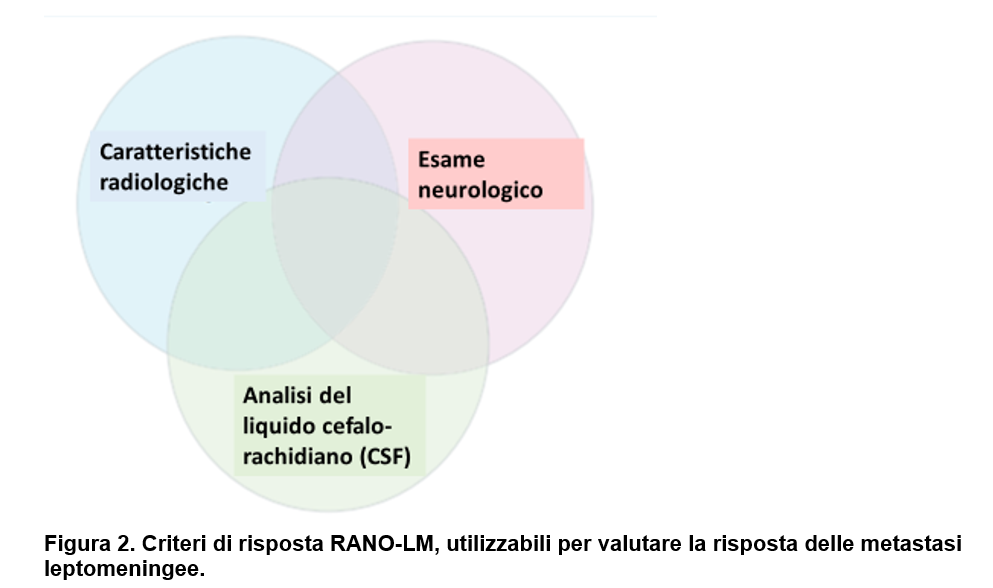
Il tasso di risposta obiettiva per LM era pari al 51,6% (33 dei 64 pazienti) con 15,6% di risposte complete (10 dei 64 pazienti), valutate dal BICR secondo i criteri RANO-LM (Figura 2).
Il tasso di risposte obiettive a livello della metastasi leptomeningee valutato invece dagli investigatori secondo i criteri RECIST v.1.1 era pari al 6,3%.
La valutazione della qualità di vita ha evidenziato un miglioramento dello stato di salute nel tempo con osimertinib ma un peggioramento alla progressione di malattia.
Le analisi farmocinetiche condotte in 49 pazienti in cui erano stati collezionati campioni di plasma e di CFS prima del 3° e del 6° ciclo, hanno evidenziato un rapporto CFS/plasma di osimertinib del 22%, a testimonianza di una penetrazione del farmaco nel SNC.
CONCLUSIONI
I risultati dello studio BLOSSOM evidenziano l’efficacia intracranica e i benefici in sopravvivenza dei 80 mg/dei di osimertinib nei pazienti con NSCLC e mutazione EGFR con metastasi leptomeningee.
Osimertinib è risultato efficace sia nei pazienti con T790M Negatività che nei pazienti con T790 Positività.
COMMENTO
Ad oggi, la valutazione della risposta obiettiva per i pazienti con metastasi leptomeningee non è stabilita: il gruppo RANO-LM ha proposto criteri descritti nel Consensus pubblicato nel 2017, criteri che prendono in considerazione tre aree: caratteristiche radiologiche, caratteristiche cliniche e l’analisi del liquido cefalo-rachidiano (Chamberlain 2017).
Nello studio BLOSSOM il tasso di risposte obiettive riportato dagli investigatori secondo i criteri RECIST v 1.1 è stato del 6,3 %, di molto inferiore al 51,6% riportato dal BICR che ha utilizzato i criteri RANO-LM.
D’altra parte, il tasso di controllo di malattia è stato sovrapponibile (81,3% vs 85,9%) così come la PFS mediana intracranica, sottolineando la necessità di validazioni future in studi prospettici, con numerosità adeguata, del sistema di valutazione secondo i criteri RANO-LM.
Bibliografia
Li Y-S, Jiang B-Y, Yang J-J, et al: Leptomeningeal metastases in patients with NSCLC with EGFR mutations. J Thorac Oncol 11:1962-1969, 2016
Chamberlain M, Junck L, Brandsma D, et al: Leptomeningeal metastases: A RANO proposal for response criteria. Neuro Oncol 19:484-492, 2016
Eisenhauer EA, Therasse P, Bogaerts J, et al: New response evaluation criteria in solid tumours: Revised RECIST guideline (version 1.1). Eur J Cancer 45:228-247, 2009
Le Rhun E, Weller M, Brandsma D, et al: EANO–ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up of patients with leptomeningeal metastasis from solid tumours. Ann Oncol 28:iv84-iv99, 2017
Si consiglia di leggere:
Chamberlain M, Junck L, Brandsma D, et al: Leptomeningeal metastases: A RANO proposal for response criteria. Neuro Oncol 19:484-492, 2016


