
FIRST-LINE NIVOLUMAB PLUS RELATLIMAB VERSUS NIVOLUMAB PLUS IPILIMUMAB IN ADVANCED MELANOMA: AN INDIRECT TREATMENT COMPARISON USING RELATIVITY-047 AND CHECKMATE 067 TRIAL DATA.
Long GV, Lipson EJ, Hodi FS, Ascierto PA, Larkin J, Lao C, Grob JJ, Ejzykowicz F, Moshyk A, Garcia-Horton V, Zhou ZY, Xin Y, Palaia J, McDonald L, Keidel S, Salvatore A, Patel D, Sakkal LA, Tawbi H, Schadendorf D.
J Clin Oncol. 2024 Nov 20;42(33):3926-3934. doi: 10.1200/JCO.24.01125. Epub 2024 Aug 13. PMID: 39137386; PMCID: PMC11575907.
Link all’articolo:
https://pubmed.ncbi.nlm.nih.gov/39137386/
Nel 2015 sono stati pubblicati i risultati dello studio clinico randomizzato di fase II-III: RELATIVITY-047 (TAWBI HA, NEJM 2015) che ha confrontato in pazienti con melanoma metastatico o non resecabile NON pretrattati, la combinazione NIVOLUMAB (anticorpo anti PD-1) e RELATLIMAB (anticorpo anti-LAG-3) rispetto a NIVOLUMAB, evidenziando un vantaggio statisticamente e clinicamente significativo della combinazione ( 10,1 mesi vs 4,63 mesi; HR= 0,75; 95% CI 0,62-0,92; p=0,006) (leggere Addendum).
Nel 2015 sono stati pubblicati i risultati dello studio randomizzato di fase III (Larkin J, NEJM 2015) che ha confrontato la combinazione nivolumab-ipilimumab versus nivolumab e versus ipilimumab, che ha evidenziato una PFS mediana di 11,5 mesi (95% CI 8,9-16,7) con la combinazione NIVO-IPI, 6, 9 mesi (95% CI 4,3-9,5) con NIVO e 2,9 mesi (95% CI 2,8-3,4) con IPI. L’HR per il confronto tra NIVO-IPI e NIVO era pari a 0,74 (95% CI 0,60-0,92). La Overall Survival , ad un follow up minimo di 36 mesi) non era ancora stata raggiunta con NIVO-IPI ed era 37,6 mesi con NIVO e 19,9 mesi con IPI (Wolcholk JD, NEJM 2017). Eventi avversi di grado 3-4 si sono verificati nel 55% dei pazienti del grauppo IPI-NIVO , nel 16,3% del gruppo NIVO e nel 27,3% del gruppo IPI (Larkin J, NEJM 2015). Nel sito di AIGOM sono stati riportati inoltre i risultati ad un follow up minimo di 10 anni:
Poiché non esiste un confronto testa a testa di Nivolumab-Ipilimumab vs Nivolumab-Relatlimab in pazienti con melanoma avanzato (metastatico e non resecabile) e poiché i confronti indiretti che hanno valutato i dati pubblicati dei trials usando analisi non aggiustate suggeriscono una efficacia simile delle due combinazioni ma un migliore profilo di tossicità per Nivolumab-Relatlimab, è stata condotta una analisi, esploratoria, di confronto indiretto di questi due trattamenti utilizzando i dati “patient-level” dello studio di fase II-III RELATIVITY-047 e dello studio di fase III, CHECKMATE 067.
METODI
L’IPTW (=inverse probability of treatment weighting) ha aggiustato le differenze delle caratteristiche basali dei pazienti.
Per questa analisi sono stati utilizzati i risultati a un follow up mediano di 33 mesi per lo studio RELATIVITY-047 e di 36 mesi per lo studio CHECKMATE067 per allineare le valutazioni dei due trials.
Gli outcomes di questa analisi includevano:
- Progression-Free Survival (PFS);
- tasso confermato di risposte obiettive (cORR);
- Sopravvivenza melanoma-specifica;
- Overall Survival;
- eventi avversi relativi ai trattamenti.
Le analisi di sottogruppo erano esploratorie.
RISULTATI
Dopo l’IPTW, le caratteristiche basali dei pazienti risultavano bilanciate per Nivolumab-Relatlimab (n=339) e per Nivolumab-Ipilimumab (n=297).
Nivolumab-Relatlimab ha dimostrato, in questo confronto indiretto, risultati simili in termini di:
- PFS (HR = 1,08 ; 95% CI 0,88-1,33);
- cORR (odds ratio 0,91; 95% CI 0,73-1,14);
- OS (HR = 0,94 ; 95% CI 0,75-1,19);
- Sopravvivenza melanoma-specifica (HR = 0,86 ; 95% CI 0,67-1,12) rispetto a Nivolumab-Ipilimumab.
Tra i sottogruppi, è stata evidenziata una maggiore differenza numerica a favore di Nivolumab-Ipilimumab per PFS nel sottogruppo con melanoma acrale; per la cORR nel sottogruppo BRAF-mutato, melanoma acrale, melanoma della mucosa e LDH > 2 volte il valore massimo normale; per la OS nel sottogruppo con melanoma acrale e nel sottogruppo con LDH > 2 volte il valore massimo normale.
D’altronde, queste analisi erano limitate dal piccolo campione numerico dei sottogruppi e dagli ampi limiti di confidenza.
La combinazione Nivolumab-Relatlimab è stata associata a minor incidenza di eventi avversi di grado 3-4 correlati al trattamento (23% vs 61% della combinazione Nivolumab-Ipilimumab) e a minor incidenza di eventi avversi di qualsiasi grado che hanno portato a interruzione del trattamento (17% vs 41%).
CONCLUSIONI
Nivolumab-Relatlimab ha dimostrato una efficacia simile a Nivolumab-Ipilimumab nella popolazione globale, inclusi la maggior parte -ma non tutti- i sottogruppi e un miglior profilo di tossicità nei pazienti con melanoma avanzato non trattato. Questi risultati vanno interpretati con cautela.
COMMENTO
In Italia, dall’autunno 2022 Ipilimumab in associazione a Nivolumab è rimborsato negli adulti e negli adolescenti di eta’ pari o superiore a dodici anni, per il trattamento del melanoma metastatico in presenza di metastasi cerebrali asintomatiche o con PD-L1< 1% (DETERMINA AIFA del 24 ottobre 2022 n. 773/2022; GU n.256 del 2-11-2022).
Da giugno 2024, Ipilimumab in associazione a nivolumab è rimborsato per il trattamento del melanoma avanzato (non resecabile o metastatico) negli adulti e negli adolescenti di eta’ pari o superiore a dodici anni (Determina AIFA n. 133/2024 del 7 giugno 2024– GU n.140 del 17-6-2024)
A seguito della pubblicazione della Determina AIFA del 5 settembre 2024 (Determina n. 466/2024) nella GU n. 220 del 19/09/2024, a partire dal 20/09/2024 è possibile utilizzare, in regime di rimborsabilità SSN, nivolumab+relatlimab per il trattamento di prima linea del melanoma avanzato (non resecabile o metastatico) negli adulti e negli adolescenti di età pari o superiore a 12 anni con espressione tumorale del PD-L1 < 1%.
Bibliografia
Tawbi HA, Schadendorf D, Lipson EJ, et al: Relatlimab and nivolumab versus nivolumab in untreated advanced melanoma. N Engl J Med 386:24-34, 2022
Tawbi HA, Hodi FS, Lipson EJ, et al: Nivolumab (NIVO) plus relatlimab (RELA) vs NIVO in previously untreated metastatic or unresectable melanoma (RELATIVITY-047): Overall survival (OS) and melanoma-specific survival (MSS) outcomes at 3 years. Presented at 2024 American Society of Clinical Oncology (ASCO) Annual Meeting. Presentation number 9524, Chicago, IL, & online, May 31- June 4, 2024
Larkin J, Chiarion-Sileni V, Gonzalez R, et al. Combined nivolumab and ipilimumab or monotherapy in untreated melanoma. N Engl J Med 2015;373:23-34.
Wolchok JD, Chiarion-Sileni V, Gonzalez R, et al. Overall survival with combined nivolumab and ipilimumab in advanced melanoma. N Engl J Med 2017; 377:1345-56.
Wolchok JD, Chiarion-Sileni V, Rutkowski P, Cowey CL, Schadendorf D, Wagstaff J, Queirolo P, Dummer R, Butler MO, Hill AG, Postow MA, Gaudy-Marqueste C, Medina T, Lao CD, Walker J, Márquez-Rodas I, Haanen JBAG, Guidoboni M, Maio M, Schöffski P, Carlino MS, Sandhu S, Lebbé C, Ascierto PA, Long GV, Ritchings C, Nassar A, Askelson M, Benito MP, Wang W, Hodi FS, Larkin J; CheckMate 067 Investigators. Final, 10-Year Outcomes with Nivolumab plus Ipilimumab in Advanced Melanoma. N Engl J Med. 2025 Jan 2;392(1):11-22. doi: 10.1056/NEJMoa2407417. Epub 2024 Sep 15. PMID: 39282897.
Margolin KA. Using Indirect Comparisons of Prospective, Randomized Trials to Make Therapeutic Decisions in Melanoma: Cross-Trial Comparisons as Surrogates for Proper Head-To-Head Studies? J Clin Oncol. 2024 Nov 20;42(33):3891-3894. doi: 10.1200/JCO-24-01634. Epub 2024 Oct 7. PMID: 39374466.

Sono stati randomizzati da maggio 2018 a dicembre 2020 (1:1) un totale di 714 pazienti: 355 nel gruppo relatlimab-nivolumab e 399 nel gruppo Nivolumab (Figura 1).
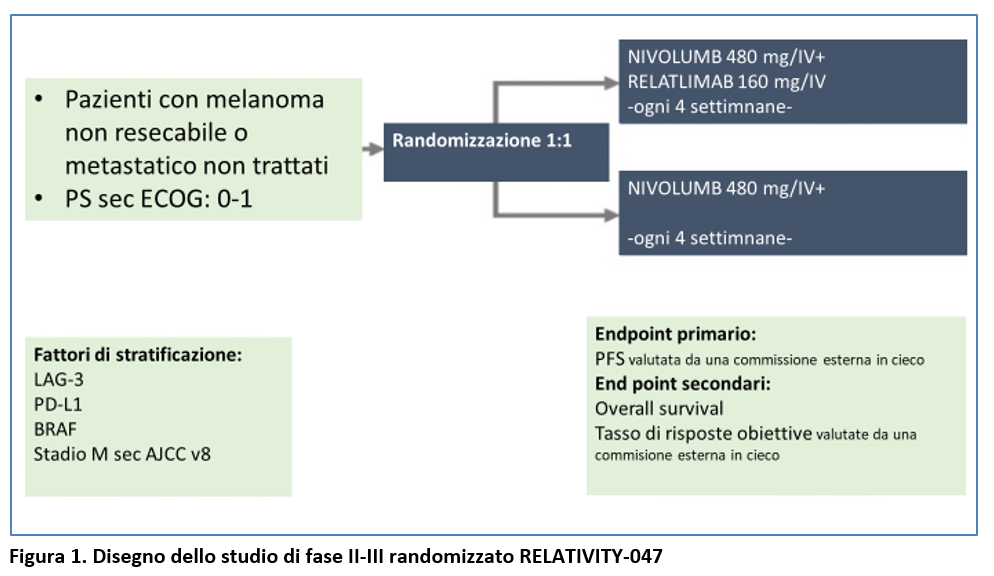
I pazienti che avevano ricevuto in (neo)-adiuvante terapie contenenti inibitori di PD-1, CTLA-4, BRAF o MEK (o una combinazione di BRAF e MEK inibitori) erano elegibili se la terapia era stata completata almeno da 6 mesi prima della data della ripresa di malattia.
I pazienti che avevano ricevuto un precedente trattamento con interferon erano elegibili se l’ultima dose era stata somministrata 6 settimane prima della randomizzazione.
Criteri di esclusione erano:
- Melanoma uveale;
- Metastasi cerebrali non trattate, attive oppure metastasi leptomeningee.
L’end point primario era la progressione-Free Survival sec. RECIST 1.1 valutata da una commissione indipendente in cieco e definito come il tempo intercorso tra la data di randomizzazione e la prima data di progressione documentata di malattia o la data del decesso per qualsiasi causa.
- Endpoint secondari comprendevano:
- Sopravvivenza globale (Overall Survival);
- Risposta obiettiva (sec RECIST v 1.1) valutata da una commissione indipendente in cieco a 12 settimane e poi ogni 8 settimane fino a 52 mesi, e poi ogni 12 settimane fino a progressione di malattia o interruzione del trattamento.
- Endpoint esplorativi includevano:
- PFS in sottogruppi pre-specificati;
- Quality of Life.
RISULTATI
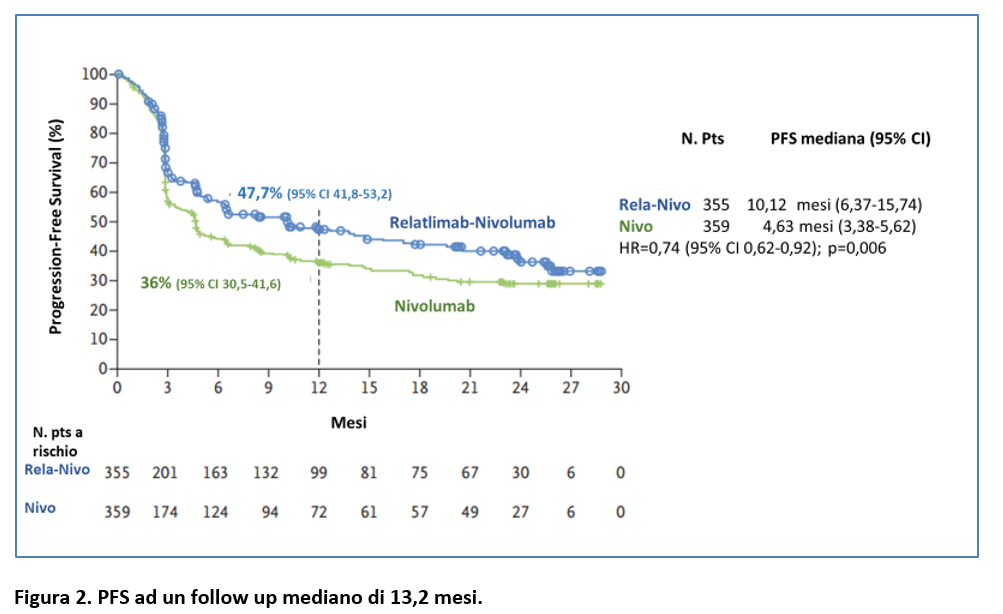
Ad un follow up mediano di 13,2 mesi (chiusura del database 09/03/2021) la PFS mediana era pari a :
- 10,1 mesi (95% CI 6,37-15,74) nel gruppo Relatlimab-Nivolumab;
- 4,63 mesi (95% CI 3,38-5,62) nel gruppo Nivolumab, con HR per rischio di progressione/morte pari a 0,75 (95% CI 0,62-0,92); p = 0,006 (Figura 2).
La PFS a 12 mesi è stata del 47,7% con la combinazione (95% CI 41,8-53,2) e del 36% (95% CI 30,5-40,6) con Nivolumab (Figura 2).
La PFS nei vari sottogruppi chiave era la migliore nel gruppo di combinazione.
SAFETY
Eventi avversi di grado 3-4 si sono verificati nel 18,9% dei pazienti del gruppo relatlimab-nivolumab e del 9,7% dei pazienti del gruppo Nivolumab, che hanno portato a interruzione del trattamento nell’8,5% dei pazienti della combinazione e nel 6,7% dei pazienti del gruppo monoterapia.
- Gli eventi avversi immuno-correlati più frequenti sono stati:
- Ipotiroidismo/tiroidite (solo grado 1/2: 18% vs 13,9%);
- Rash (q.si grado: 9,3% vs 6,7%);
- Diarrea/colite (q.si grado 6,8% vs 3,1%).
- Miocardite si è verificata nell’1,7% dei pazienti del gruppo di combinazione relatlimab-nivolumab e nello 0,6% dei pazienti del gruppo nivolumab.
Ad un follow up mediano di 33,8 mesi (TAWBI H.A., Asco Meeting 2024) la PFS (HR = 0,79 ; 95% CI 0,66-0,95) e la OS (HR = 0,80 ; 95% CI 0,66-0,99) erano consistenti con quanto precedentemente riportato.

