
DURVALUMAB AFTER CHEMORADIOTHERAPY IN LIMITED-STAGE SMALL-CELL LUNG CANCER.
Cheng Y, Spigel DR, Cho BC, Laktionov KK, Fang J, Chen Y, Zenke Y, Lee KH, Wang Q, Navarro A, Bernabe R, Buchmeier EL, Chang JW, Shiraishi Y, Goksu SS, Badzio A, Shi A, Daniel DB, Hoa NTT, Zemanova M, Mann H, Gowda H, Jiang H, Senan S; ADRIATIC Investigators.
N Engl J Med. 2024 Sep 13. doi: 10.1056/NEJMoa2404873
Dal 21 Novembre 2024 durvalumab è disponibile in Italia nell’ambito di un EAP nei pazienti con microcitoma polmonare malattia limitata, che abbiano ricevuto trattamento di chemioterapia contenente platino e radioterapia, sulla base dei risultati dello studio di fase 3 ADRIATIC.
Il microcitoma polmonare (SCLC) rappresenta il 15% di tutti i tumori del polmone e in circa un terzo delle diagnosi la malattia è limitata. Nello SCLC malattia limitata, una più lunga sopravvivenza è ottenuta con chemio-radioterapia toracica concomitante e un precoce inizio della radioterapia toracica, seguita da radioterapia encefalica profilattica (quando indicato). D’altra parte, la maggiore parte dei pazienti presenta una ripresa di malattia nei due anni dall’inizio del trattamento, e la sopravvivenza globale a 5 anni varia dal 29% al 34%.
Durvalumab è un anticorpo monoclonale anti-PD-L1 che nel trial di fase 3 PACIFIC in pazienti con tumore polmonare non microcitoma (NSCLC) stadio III non resecabile che avevano ricevuto chemio-radioterapia concomitante toracica (chemioterapia contenente platino) ha dimostrato, somministrato quale mantenimento, di aumentare significativamente la PFS e la OS, rispetto a placebo, (Spigel DR, 2022).
Nel microcitoma malattia estesa, i risultati dello studio di fase 3 CASPIAN hanno evidenziato che durvalumab aggiunto allo schema chemioterapico classico con platino + etoposide ha aumentato in maniera significativa la OS in pazienti non pretrattati (Paz-Ares L, 2019), diventando così lo standard di trattamento nello SCLC con malattia estesa.
Nello studio di fase 3 ADRIATIC è stato valutato durvalumab (con o senza tremelimumab, un anticorpo anti-CTLA-4) rispetto a placebo come terapia di mantenimento dopo risposta o stabilizzazione a chemio-radioterapia concomitante nei pazienti con SCLC malattia limitata. In questo articolo vengono riportati i risultati della 1a analisi ad interim della OS e della PFS di durvalumab versus placebo.
I risultati nel gruppo durvalumab + tremelinumab rimangono “blinded”.
METODI
Erano eleggibili per lo studio ADRIATIC i pazienti con SCLC malattia limitata (documentata isto-o citologicamente) stadio I-II-III (i pazienti stadio I o II dovevano avere una malattia non operabile) secondo la 8a edizione AJCC Cancer Staging Manual, senza progressione dopo chemio-terapia concomitante e definitiva.
La radioterapia doveva iniziare non oltre la fine del 2° ciclo di chemioterapia (Figura 1).
In questo studio randomizzato multicentrico in doppio cieco, placebo-controllato, i pazienti erano stati inizialmente randomizzati (1:1:1) a ricevere:
- Durvalumab
- Durvalumab + tremelimumab
- Placebo (Figura 1).
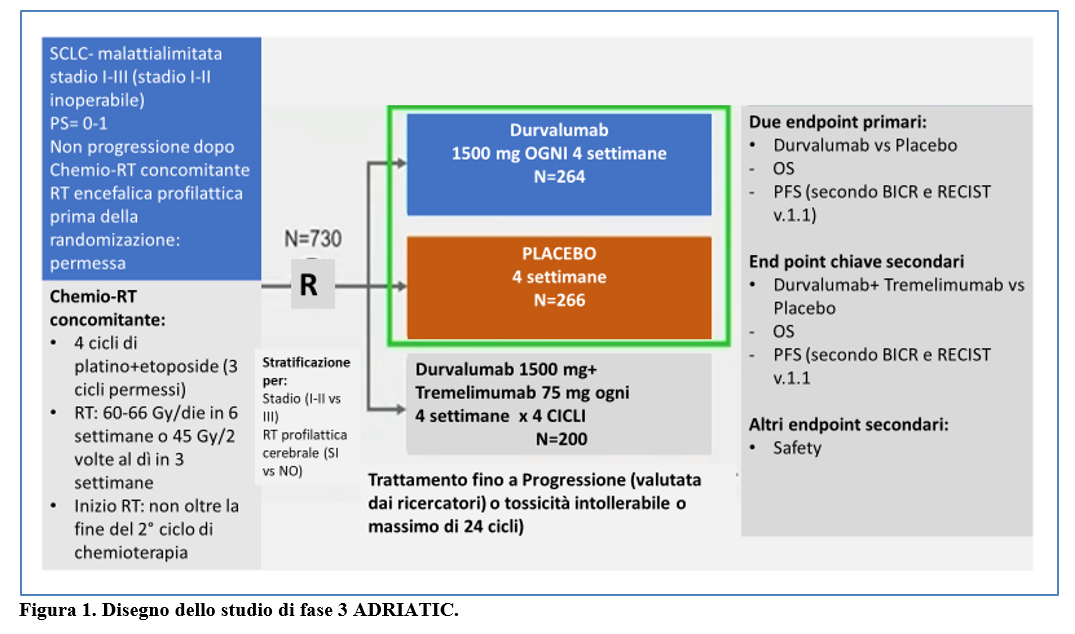
Dopo un emendamento del Novembre 2020, i pazienti sono stati randomizzati 1:1 e ricevere durvalumab oppure placebo. La randomizzazione e l’avvio del trattamento avvenivano entro 42 giorni dal termine della chemioterapia, con stratificazione in base allo stadio (I-II versus III) e alla RT encefalica profilattica (SI vs NO).
I due endpoint primari erano la OS e la PFS del gruppo durvalumab versus gruppo placebo.
La PFS è stato valutata sulla base di una revisione centralizzata indipendente, in cieco, secondo i RECIST v.1.1.
Tra gli endpoint secondari riportati in questo articolo, ci sono:
-Risposta obiettiva;
-PFS a 18 e a 24 mesi:
-OS a 24 mesi e a 36 mesi;
-incidenza di eventi avversi.
RISULTATI
Tra Settembre 2018 e Agosto 2021, sono stati arruolati 939 pazienti e sono stati randomizzati 730 pazienti a ricevere durvalumab (=264), durvalumab + tremelinumab (=200) o placebo (=206) (intention-to-treat-population). Sono stati arruolati 600 pazienti prima dell’emendamento e 130 dopo.
I dati riportati sono relativi a un totale di 530 pazienti nell’intention-to-treat (ITT) population.
Le caratteristiche dei pazienti al basale erano ben bilanciate tra il gruppo durvalumab e il gruppo placebo (Tabella 1 e 2).
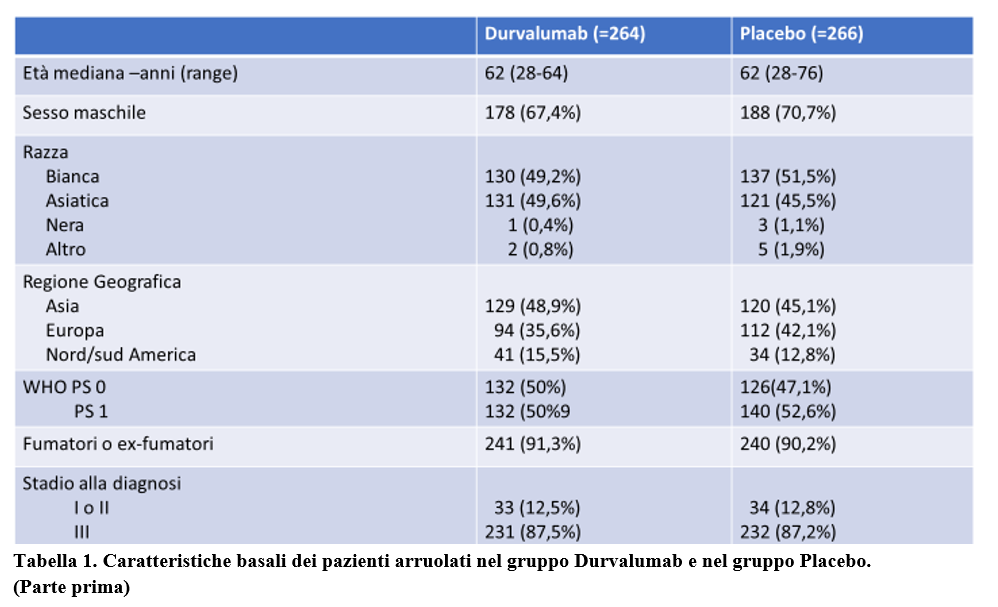
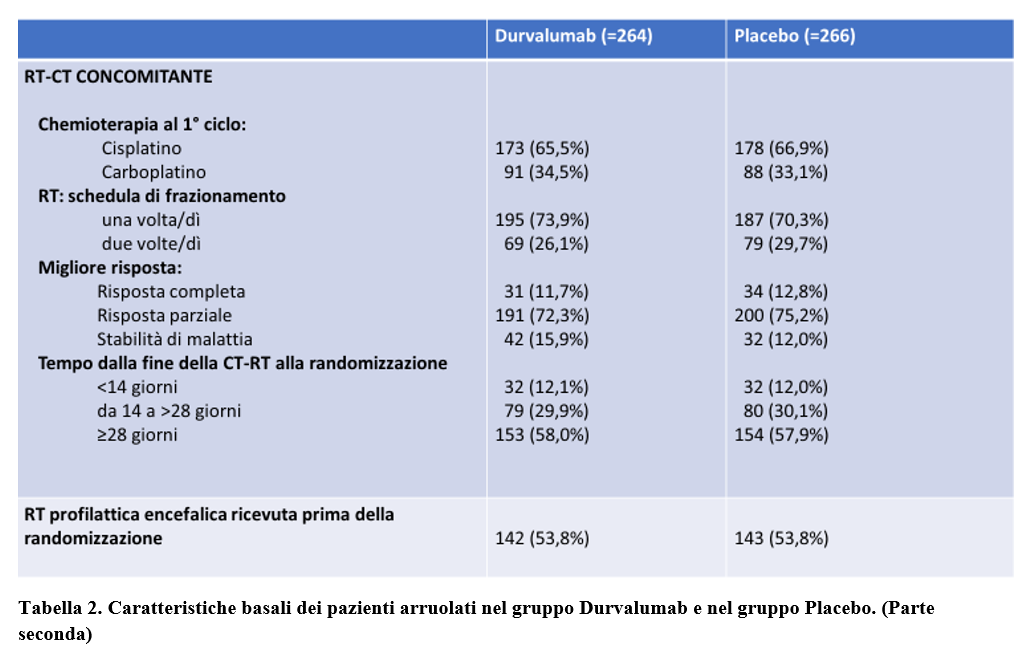
L’età mediana dei pazienti era 62 anni; il 68,5% erano ex-fumatori e il 22% fumatori; la maggior parte (87,4%) aveva uno stadio III di malattia alla diagnosi.
Alla data del cutoff per l’analisi dei dati (15 gennaio 2024) 261 pazienti erano deceduti (49,2%).
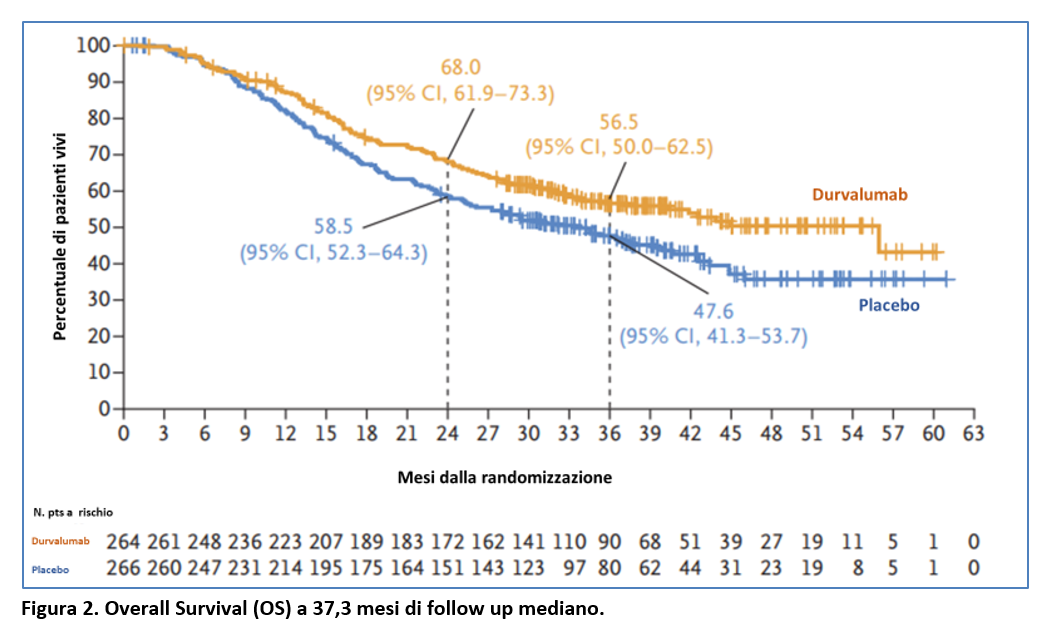
Ad un follow up per la OS di 37,2 mesi mediano, la OS è stata significativamente più lunga nel gruppo durvalumab che nel gruppo placebo (55,9 mesi vs 33,4 mesi; stratified HR for death= 0,73; 98,321% CI; 0,54-0,98; p = 0,01) (Figura 2).
La OS a 24 mesi è stata del 68% nel gruppo durvalumab e del 58,5% nel gruppo placebo e la OS a 36 mesi è stata del 56,5% e del 47,6% nei due gruppi, rispettivamente (Figura 2).
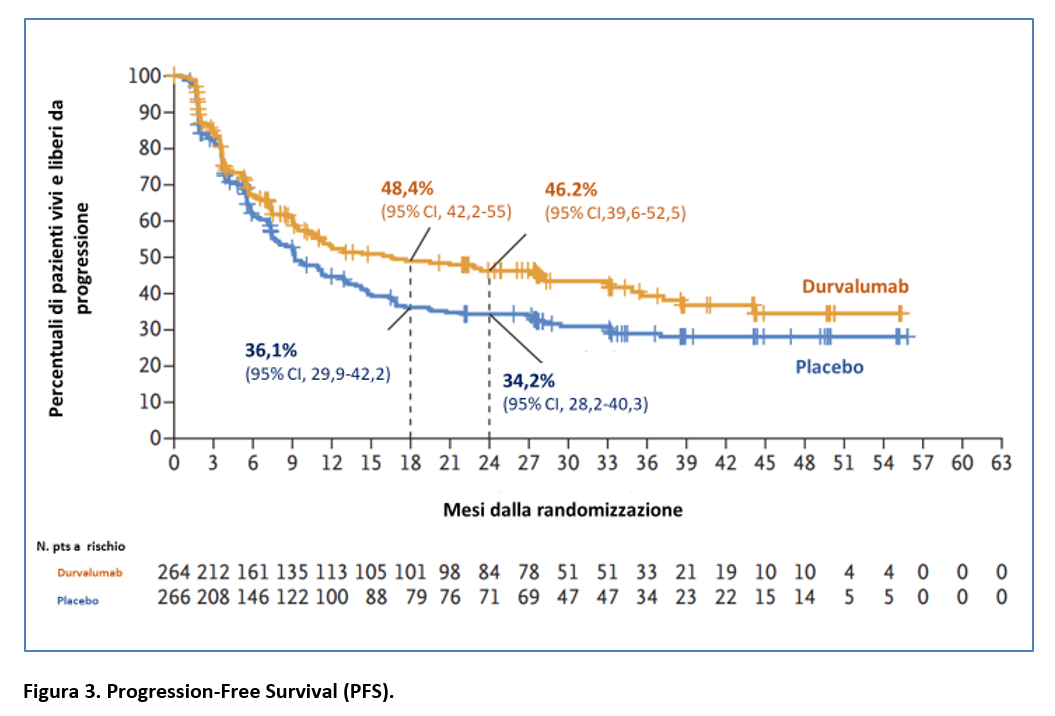
Ad un follow up di oltre 27 mesi per la PFS (308 pazienti avevano avuto una progressione di malattia o erano deceduti; 58,1%), la PFS mediana è stata significativamente più lunga nel gruppo durvalumab (16,6 mesi) che nel gruppo placebo (9,2 mesi) con “stratifical” HR per progressione o morte dello 0,76 (95,195% CI; 0,59-0,98; p = 0,02) (Figura 3).
La PFS a 18 mesi e a 24 mesi è stata pari a 48,8% e 46,2% nel gruppo durvalumab rispetto al 36,1% e al 34,2% nel gruppo placebo (Figura 3).
SAFETY
L’incidenza di eventi avversi di grado 3 o di grado 4 è stata del 24,4% nei pazienti che ricevevano durvalumab e del 24,2% nei pazienti che ricevevano placebo.
Gli eventi avversi hanno portato a interruzione del trattamento il 16,4% e il 10,6% dei pazienti, rispettivamente, e a morte il 2,7% e l’1,9%.
Polmoniti o polmoniti da radioterapia di grado 3/4 si sono verificate nel 3,1% dei pazienti del gruppo durvalumab e nel 2,6% dei pazienti del gruppo placebo.
CONCLUSIONI
La terapia adiuvante con durvalumab ha determinato una più lunga OS e PFS rispetto a placebo nei pazienti con microcitoma polmonare a malattia limitata, con buon profilo di tossicità.
COMMENTO a cura di Angelo Delmonte (IRCCS Istituto Romagnolo per lo Studio dei Tumori “Dino Amadori” (IRST), Meldola (FC)
Il microcitoma polmonare è rimasto per anni una delle patologie oncologiche di più difficile gestione, sia per la sua aggressività che per l’esiguità di opzioni terapeutiche. Contrariamente poi a quanto visto nel NSCLC, le conoscenze biologiche della malattia sono agli albori, sebbene in recente evoluzione. L’introduzione pertanto dell’immunoterapia rappresenta la vera novità terapeutica nell’arco di molti anni, in prima battuta nella malattia estesa e ora anche in quella limitata grazie allo studio di Fase III ADRIATIC randomizzato, placebo-controllato, in doppio cieco.
L’utilizzo infatti di durvalumab, noto anti-PDL1 da tempo in uso anche nel NSCLC, come mantenimento dopo chemioterapia platino-basata concomitante a radioterapia è in grado di migliorare sia la sopravvivenza globale che quella libera da progressione con HR statisticamente significativi e clinicamente rilevanti. Ciò si traduce in una percentuale incrementale di pazienti globalmente sopravviventi a 36 mesi (56.5% vs 47.6%) e liberi da progressione a 24 mesi (46.2% vs 34.2%), con un forte impatto sulla pratica clinica quotidiana. Peraltro poi all’ESMO meeting 2024 sono stati mostrati da Sursh Senan del Cancer Center di Amsterdam le analisi per sottogruppo (Senan S et al, Ann Oncol 2024)i. L’attività di durvalumab si mantiene efficace e rilevante indipendentemente che si utilizzi cisplatino o carboplatino, che si esegua o meno la PCI, che si esegua uno schema di radioterapia mono- o bi-giornaliero. Questi dati, la cui pubblicazione in extenso è attesa nel prossimo futuro, sono di particolare rilevanza, poiché lasciano campo a “semplificazioni” terapeutiche che possano venire incontro alla real world practice.
In merito al profilo di sicurezza poi l’aggiunta di durvalumab appare sicuro, aggiungendo quei tipi di tossicità proprie dell’immunoterapia sebbene senza un’incidenza maggiore che nel braccio di controllo. L’incidenza di polmoniti iatrogene, l’evento avverso più temuto in questo contesto, non differisce poi nei due bracci di trattamento. Tali dati confortano quindi nell’utilizzo di questo schema di terapia da affrontarsi secondo l’abituale pratica clinica già in essere.
Lo studio ADRIATIC, in modo a quanto già fatto dallo studio PACIFIC per il NSCLC localmente avanzato, definisce quindi il nuovo standard di trattamento per il SCLC con estensione limitata con risultati per la prima volta da anni clinicamente rilevanti. Molto tuttavia rimane ancora da fare per ottimizzare la selezione del paziente e migliorare ulteriormente i tassi di risposta e sopravvivenza in una malattia che rimane tuttora uno dei medical need oncologici più rilevanti.
Dal 21 Novembre 2024 durvalumab è disponibile in Italia nell’ambito di un EAP nei pazienti con microcitoma polmonare malattia limitata, che abbiano ricevuto trattamento di chemioterapia contenente platino e radioterapia.
Attualmente, durvalumab (nome commerciale ) è rimborsato in Italia con la seguente indicazione: «”Imfinzi” in associazione con etoposide e carboplatino o cisplatino e’ indicato per il trattamento di prima linea di pazienti adulti con carcinoma polmonare a piccole cellule in stadio esteso ES-SCLC).»
BIBLIOGRAFIA
Spigel DR, Faivre-Finn C, Gray JE, et al. Five-Year Survival Outcomes From the PACIFIC Trial: Durvalumab After Chemoradiotherapy in Stage III Non-Small-Cell ung Cancer. J Clin Oncol 2022;40:1301-11
Paz-Ares L, Dvorkin M, Chen Y, et al. Durvalumab plus platinum-etoposide versus platinum-etoposide in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): a randomised, controlled, open-label, phase 3 trial. Lancet 2019;394:1929-39.
Senan S et al. Durvalumab as consolidation therapy in limited-stage SCLC (LS-SCLC): outocmes by prior concurrent chemoradiothrapy (cCRT) regimen and prophylactic cranial irradiation (PCI) use in the ADRIATIC trial. ESMO Congress 2024, LBA81.
Annals of Oncology (2024) 35 (suppl_2): 1-72


