
OVERALL SURVIVAL WITH PEMBROLIZUMAB IN EARLY-STAGE TRIPLE-NEGATIVE BREAST CANCER.
Schmid P, Cortes J, Dent R, McArthur H, Pusztai L, Kümmel S, Denkert C, Park YH, Hui R, Harbeck N, Takahashi M, Im SA, Untch M, Fasching PA, Mouret-Reynier MA, Foukakis T, Ferreira M, Cardoso F, Zhou X, Karantza V, Tryfonidis K, Aktan G, O’Shaughnessy J; KEYNOTE-522 Investigators.
N Engl J Med. 2024 Sep 15. doi: 10.1056/NEJMoa2409932.
Link all’abstract: https://pubmed.ncbi.nlm.nih.gov/39282906/
L’impiego di pembrolizumab nell’ambito del trattamento neoadiuvante del carcinoma mammario triplo negativo (stadi II-III) è autorizzato da EMA e da AIFA (Determina 10 luglio 2023, GU 18/07/2023 Serie Generale n. 166) ed è rimborsato dal Servizio Sanitario Nazionale italiano con la seguente indicazione:
“in associazione a chemioterapia come trattamento neoadiuvante e poi continuato in monoterapia come trattamento adiuvante dopo intervento chirurgico per pazienti con carcinoma mammario triplo negativo localmente avanzato o in fase iniziale ad alto rischio di recidiva (cT1c cN1-N2; cT2-4 cN0-N2)”.
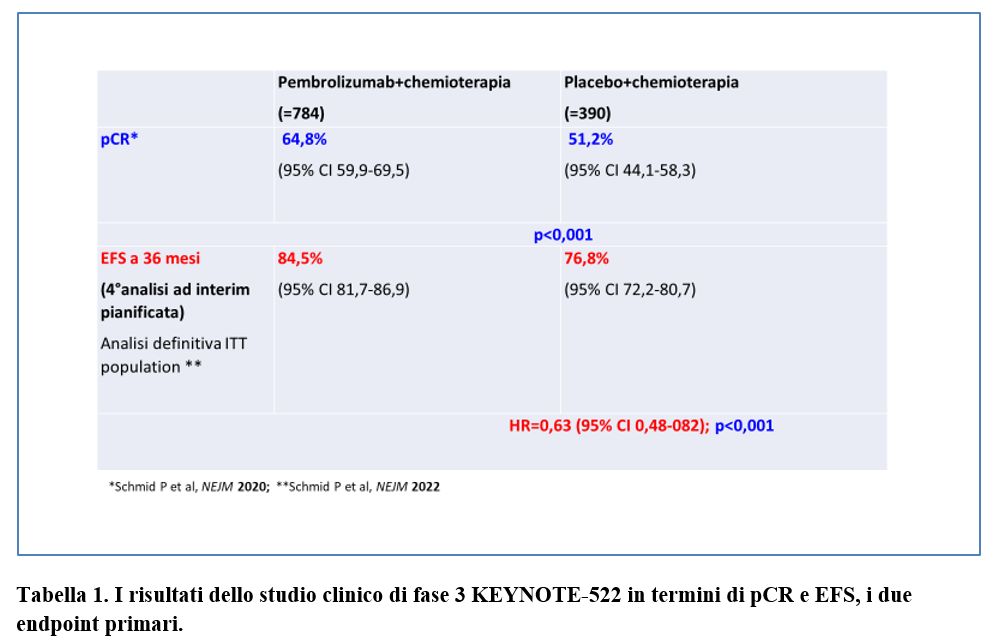
Questa indicazione si basa sui risultati dello studio KEYNOTE-522 (Schmid P, 2020; Schmidt P, 2022) che, da marzo 2017 a settembre 2018, ha randomizzato (2:1) 1.174 pazienti con carcinoma mammario triplo negativo mammario a ricevere in neo-adiuvante pembrolizumab-chemioterapia (=784) oppure placebo-chemioterapia (=390) (Tabella 1). I due end point co-primari erano il tasso di pCR alla chirurgia definitiva e l’EFS.
La pCR era definita come ypTO/Tis ypNO al momento della chirurgia definitiva.
La EFS era definita come il tempo intercorso tra randomizzazione e progressione di malattia che precludeva la chirurgia definitiva, ripresa locale o a distanza, secondo cancro primitivo o la morte per qualsiasi causa.
Nella Tabella 1 sono riportarti i risultati relativi agli endpoint primari.
Il KEYNOTE-522 ha evidenziato, nel setting neo-adiuvante, un beneficio statisticamente e clinicamente significativo di pembrolizumab+ chemioterapia rispetto a placebo+chemioterapia in termini di tassi di pCR e di EFS (i due endpoint primari dello studio).
erano la risposta completa patologica(pCR) e la sopravvivenza libera da eventi (Event-free SURVIVAL- EFS).

In una analisi esploratoria pre-specificata del KEYNOTE-522, è stata valutata l’Event-Free Surival (EFS) nelle varie categorie di malattia residua ( in base all’indice RBC- Residual Cancer Breast) al momento della chirurgia per tutti i pazienti. Questa analisi è stata pubblicata da Pusztai L, 2024 ed è scaricabile al link: https://www.aigom.it/2024/04/18/event-free-survival-by-residual-cancer-burden-with-pembrolizumab-in-early-stage-triple-negative-breast-cancer-tnbc-exploratory-analysis-from-keynote-522/
L’analisi ha evidenziato un beneficio con pembrolizumab in pazienti con carcinoma mammario triplo negativo che hanno ottenuto una pCR (RCB-0) e tra i pazienti con malattia residua RCB-1 e RCB-2. Il beneficio è risultato essere più pronunciato nella categoria RCB-2, che rappresenta anche la frazione maggiore (55%) di pazienti con malattia residua. Il piccolo sottogruppo di pazienti della categoria RCB-3 (malattia residua estesa) ha avuto una peggiore prognosi in entrambi i gruppi di trattamento, suggerendo che questa categoria rappresenta un sottogruppo di tumore resistente al trattamento che necessita di ulteriori terapie e ulteriori studi.
IN QUESTO ARTICOLO pubblicato sul NEJM a SETTEMBRE 2024 VIENE RIPORTATA LA SOPRAVVIVENZA GLOBALE del KEYNOTE-522.
In questo articolo pubblicato a settembre 2024 viene riportata la Overall Survival (end point secondario chiave dello studio KEYNOTE-522) alla settima analisi ad interim pre-pianificata dopo circa 84 mesi dalla randomizzazione del primo paziente (data-cutoff dei dati: 22 marzo 2024). L’analisi è stata condotta sull’ITT-population (che includeva tutti i pazienti randomizzati).
Alla data del 22 marzo 2024, 200 pazienti (67,3%) erano deceduti: 115 (14,7%) nel gruppo pembrolizumab+chemioterapia e 85 (21,8%) nel gruppo placebo+chemioterapia.
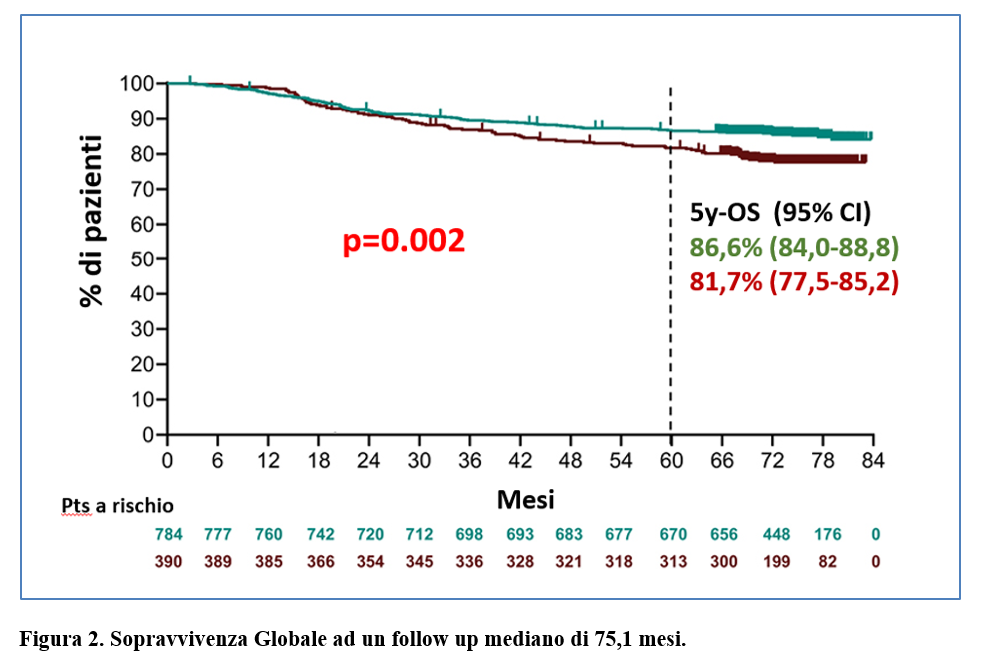
In accordo al criterio statistico pre-specificato di livello di alfa pari a 0,00503, ad un follow up mediano di 75,1 mesi è stato osservato un significativo aumento della Overall Survival nel gruppo trattato con pembrolizumab+chemioterpia rispetto al gruppo placebo+chemioterapia (Figura 2).
Gli eventi avversi sono stati in linea con i profili di tossicità già noti di pembrolizumab e chemioterapia
CONCLUSIONI
Un trattamento comprendente pembrolizumab+chemioterapia seguito da chirurgia e pembrolizumab adiuvante determina anche un significativo aumento della sopravvivenza globale, rispetto al gruppo di controllo con sola chemioterapia neo-adiuvante, in pazienti con carcinoma mammario triplo negativo.
BIBLIOGRAFIA
1-Schmid P, Cortes J, Pusztai L et al. Pembrolizumab for early triple-negative breast cancer. N Engl J Med 2020; 382: 810-821
2- Schmid P, Cortes J, Dent R et al. Event-free survival with pembrolizumab in early triple negative breast cancer. N Engl J Med 2022; 386: 556-567.
3- EVENT-FREE SURVIVAL BY RESIDUAL CANCER BURDEN WITH PEMBROLIZUMAB IN EARLY-STAGE TRIPLE NEGATIVE BREAST CANCER (TNBC): EXPLORATORY ANALYSIS FROM KEYNOTE-522.
Pusztai L, et al. Ann Oncol 2024 Feb 17:S0923-7534(24)00046-2. doi: 10.1016/j.annonc.2024.02.002.
Sintesi di questo articolo scientifico è scaricabile al sito web di AIGOM:


