
CORTICOSTEROIDS FOR IMMUNE-RELATED ADVERSE EVENTS AND CHECKPOINT INHIBITOR EFFICACY: ANALYSIS OF SIX CLINICAL TRIALS.
Verheijden RJ, de Groot JS, Fabriek BO, Hew MN, May AM, Suijkerbuijk KPM.
J Clin Oncol. 2024 Aug 7:JCO2400191. doi: 10.1200/JCO.24.00191.
Alcuni studi retrospettivi hanno evidenziato che il trattamento immunosoppressivo degli eventi avversi da inibitori del checkpoint immunitario con l’utilizzo di alte dosi di picco di corticosteroidi e/o farmaci immunosoppressivi di 2° linea possono avere un effetto detrimentale sulla sopravvivenza dei pazienti con melanoma (Bai X. 2021; Verheijden R.J. 2020; Verheijden R.J. 2024; Verheijden R.J. 2023).
In questo laoro è stato valutato se dosi picco di corticosteroidi, la dose cumulativa di corticosteroidi e/o l’uso di farmaci immunosoppressori di seconda linea fossero associati con una ridotta sopravvivenza nei pazienti trattati con la combinazione di anti-PD-1+ anti-CTLA-4 in studi clinici prospettici di fase II-III in vari tipi di tumori.
METODI
Sono stati selezionati studi clinici di fase II-III condotti in tumori per i quali la combinazione di anti-PD-1+ anti-CTLA-4 aveva ricevuto da EMA una approvazione entro dicembre 2022.
Sono stati inclusi in questo studio i pazienti che hanno ricevuto una immunosoppressione per eventi avversi correlati al trattamento con anti-PD-1 + anti-CTLA-4. Non sono stati inclusi i pazienti che hanno ricevuto una supplementazione di glicocorticoidi pari a una dose giornaliera massima equivalente a 10 mg di prednisolone per ipocortisolismo, ipopitituarismo o ipofisite.
La dose picco di corticosteroidi (dose massima al giorno 1) e la dose cumulativa di corticosteroidi (somma di tutte le dosi giornaliere) sono state calcolate in milligrammi prednisolone-equivalente.
OUTCOMES
La sopravvivenza globale (OS) è stata definita come il tempo intercorso tra l’inizio della immunosoppressione per eventi avversi da trattamento e il decesso.
La PFS (Progression-Free-Survival) è stata definita come il tempo intercorso tra l’inizio dell’immunosoppressione per eventi avversi da trattamento e la progressione di malattia (riportata dagli investigatori) o la morte per qualsiasi causa.
I pazienti erano “censored”se vivi (e liberi da progressione) all’ultimo follow up.
Per la sopravvivenza tumore-specifica, i pazienti erano “censored” nel caso di morte non correlata alla progressione di malattia.
Per valutare l’associazione di corticosteroidi e immunosoppressione di seconda linea con la sopravvivenza, l’HR aggiustato (HRadj) è stato stimato utilizzando la regressione multivariata del rischio proporzionale di Cox che includeva sesso ed età e, nelle analisi di sensibilità, il grado di eventi avversi da trattamento, il tipo di evento avverso e la ripresa di terapie con inibitori del checkpoint immunitario.
RISULTATI
I dati sono stati estratti da 6 studi clinici di fase II-III che hanno valutato la combinazione di anti-PD-1+ anti-CTLA-4 (Larkin J, 2015; Overman MJ, 2018; Motzer RJ, 2018;Doki Y, 2022; Baas P, 2021; Paz-Ares L, 2021).
Un totale di 1959 pazienti avevano ricevuto almeno una dose di immuterapia di combinazione all’interno di 6 studi Checkmate che hanno valutato Nivolumab + ipilimumab nel melanoma, nel cancro del colon-retto con MSI-H/dMMR, nel carcinoma renale avanzato, nel carcinoma esofageo squamoso avanzato, nel mesotelioma pleurico e nel NSCLC (Tabella 1).
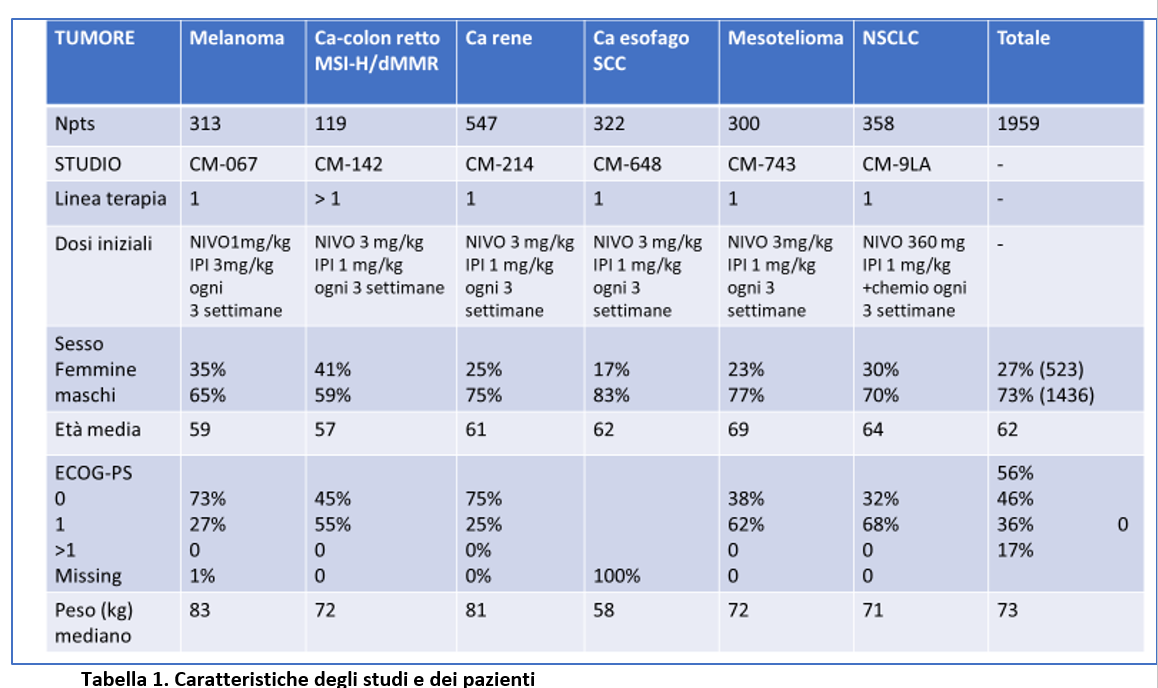
Le dosi di nivolumab e di ipilimumab erano differenti nei vari studi (Tabella 1). Sebbene le indicazioni per la somministrazione di immunosoppressione fossero simili nei vari protocolli di studio, erano generalmente raccomandate dosi più alte di corticosteroidi nel Checkmate-067 (melanoma) che negli altri trials.
Ad un follow up mediano dall’inizio di nivolumab + ipilimumab di 24 mesi, 834 pazienti (43%) avevano ricevuto una terapia sistemica immunosoppressiva per eventi avversi correlati alla terapia. La maggioranza di questi pazienti erano uomini (597; 72%) e con età media di 62 anni (Tabella 2A).
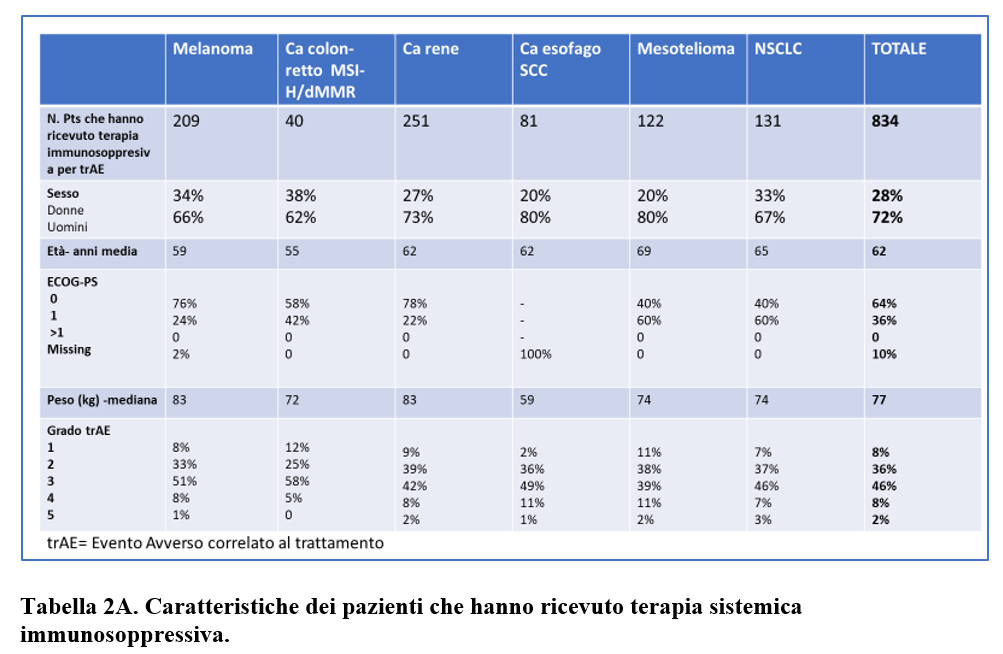
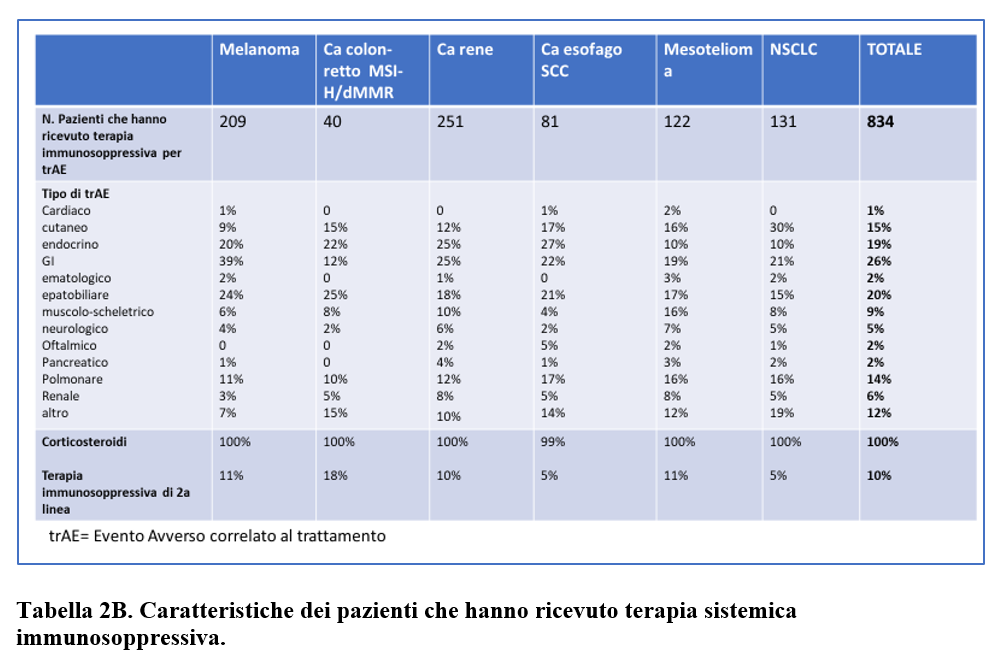
Terapia con corticosteroidi è stata somministrata nel 100% dei pazienti e una terapia sistemica immunosoppressiva di 2a linea nel 10% dei pazienti.
L’alta dose picco di corticosteroidi era associata con una peggiore PFS: l’HRadj era pari a 1,15 (95% CI : 1,02-1,29) per 1 mg/kg di prednisolone versus 0,5 mg/kg di prednisolone e l’ HRadj era pari a 1,43 (95% CI : 1,05-1,96) per 2 mg vs 0,5 mg/kg.
Effetti simili sono stati osservati per la sopravvivenza globale: HRadj è stato pari a 1,21 (95% CI : 1,06-1,39) per 1 mg/kg vs 0,5 mg/kg di prednisolone e l’HRadj è stato di 1,66 (95% CI : 1,17-2,37) per 2 mg/kg vs 0,5 mg/kg.
La dose cumulativa di corticosteroidi non era associata con la sopravvivenza. L’HRadj dell’uso di terapia sistemica immunosoppressiva di 2a linea è stata pari a 1,23 (95% CI : 0,90-1,68) per la PFS e 1,25 (95% CI : 0,83-1,77) per la OS.
CONCLUSIONI
Una più alta dose picco di corticosteroidi per il trattamento degli effetti collaterali da terapia con inibitori del checkpoint immunitario è risultata essere associata con una peggiore sopravvivenza in vari tipi di tumore, mentre non è stata evidenziata una correlazione con la dose cumulativa di steroidi.
I pazienti che hanno ricevuto una 2a linea di immunosoppressione sono stati troppo pochi per valutarne l’associazione con la sopravvivenza.
BIBLIOGRAFIA
Bai X, Hu J, Betof Warner A, et al: Early use of high-dose glucocorticoid for the management of irAE is associated with poorer survival in patients with advanced melanoma treated with anti-PD-1 monotherapy. Clin Cancer Res 27:5993-6000, 2021
Verheijden RJ, May AM, Blank CU, et al: Association of anti-TNF with decreased survival in steroid refractory ipilimumab and anti-PD1-treated patients in the Dutch Melanoma Treatment Registry. Clin Cancer Res 26:2268-2274, 2020
Verheijden RJ, Burgers FH, Janssen JC, et al: Corticosteroids and other immunosuppressants for immune-related adverse events and checkpoint inhibitor effectiveness in melanoma. Eur J Cancer 10.1016/j.ejca.2024.114172 [epub ahead of print on June 15, 2024]
Verheijden RJ, Janssen JC, Putker AE, et al: 1157P corticosteroids and second-line immunosuppressants for immune-related adverse events and melanoma survival. Ann Oncol 34:S690-S691, 2023 10.
Larkin J, Chiarion-Sileni V, Gonzalez R, et al: Combined nivolumab and ipilimumab or monotherapy in untreated melanoma. N Engl J Med 373:23-34, 2015
Overman MJ, Lonardi S, Wong KYM, et al: Durable clinical benefit with nivolumab plus ipilimumab in DNA mismatch repair–deficient/microsatellite instability–high metastatic colorectal cancer. J Clin Oncol 36:773-779, 2018
Motzer RJ, Tannir NM, McDermott DF, et al: Nivolumab plus ipilimumab versus sunitinib in advanced renal-cell carcinoma. N Engl J Med 378:1277-1290, 2018
Doki Y, Ajani JA, Kato K, et al: Nivolumab combination therapy in advanced esophageal squamous-cell carcinoma. N Engl J Med 386:449-462, 2022
Baas P, Scherpereel A, Nowak AK, et al: First-line nivolumab plus ipilimumab in unresectable malignant pleural mesothelioma (CheckMate 743): A multicentre, randomised, open-label, phase 3 trial. Lancet 397:375-386, 2021
Paz-Ares L, Ciuleanu TE, Cobo M, et al: First-line nivolumab plus ipilimumab combined with two cycles of chemotherapy in patients with non-small-cell lung cancer (CheckMate 9LA): An international, randomised, open-label, phase 3 trial. Lancet Oncol 22:198-211, 2021
COMMENTO
È fondamentale una gestione accurata degli effetti collaterali della immunoterapia. Per ulteriori informazioni, consultare la LINEA GUIDA “Gestione della Tossicità da immunoterapia” AIOM 2023, coordinata da Alessandro Inno, al seguente link:
https://www.iss.it/documents/20126/8403839/LG+200_Tox+da+immunoterapia_ed2023.pdf/703bb77e-5567-6675-8168-f3d0cddd1e4c?t=1696845726727
Link all’abstract
https://pubmed.ncbi.nlm.nih.gov/39110922/


