
PEMBROLIZUMAB PLUS CARBOPLATIN AND PACLITAXEL AS FIRST-LINE THERAPY FOR RECURRENT/METASTATIC HEAD AND NECK SQUAMOUS CELL CARCINOMA (KEYNOTE-B10): A SINGLE-ARM PHASE IV TRIAL.
Dzienis M, Cundom J, Fuentes CS, Spreafico A, Nordlinger M, Pastor AV, Alesi E, Neki A, Fung AS, Figueiredo Lima IP, Oppelt P, da Cunha Junior GF, Burtness B, Franke FA, Tseng JE, Joshi A, McCarthy J, Swaby R, Sidi Y, Gumuscu B, Naicker N, de Castro G Jr.
J Clin Oncol. 2024 Sep 1;42(25):2989-2999. doi: 10.1200/JCO.23.02625.
FREE Full Test- PMC: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC11361359/
Il trattamento di prima linea del carcinoma del testa-collo in ripresa o metastatico è rappresentato dal pembrolizumab + platino+ fluorouracile, in considerazione del vantaggio in sopravvivenza globale evidenziato dallo studio di fase III KEYNOTE-048 rispetto a cetuximab+ chemioterapia (BURTNESS B. , Lancet 2019).
D’altra parte, molti pazienti non tollerano il fluorouracile a causa della tossicità gastrointestinali e cardiovascolari; inoltre i pazienti con deficienza della di-idro-pirimidina deidrogenasi (3-5% della popolazione generale) sono più suscettibili agli eventi avversi correlati al fluorouracile e, in aggiunta, il trattamento con fluorouracile può essere collegato a eventuali complicanze collegate al posizionamento e utilizzo di cateteri necessari per permettere l’infusione continua endovenosa di 4 giorni del farmaco.
Per ridurre le tossicità e le problematiche legate alla somministrazione di fluorouracile in infusione, è stato disegnato uno studio di fase IV-KEYNOTE-B10- a braccio singolo, open-label, multicentrico che ha valutato l’efficacia e la safety di pembralizumab, paclitaxel e carboplatino come prima linea in pazienti con carcinoma squamocellulare ricorrente o metastatico.
METODI
KEYNOTE-B10 è uno studio a braccio singolo, open-label, multicentrico, di fase IV, condotto in 33 centri in Argentina, Australia, Brasile, Canada e Stati Uniti. I pazienti elegibili avevano età ≥ 18 anni con diagnosi isto-/cito-logicamente confermata di carcinoma squamocellulare testa-collo ricorrente/metastatico considerato non suscettibile di terapie locali e non trattati precedentemente con terapia sistemica antitumorale nel setting ricorrente/metastatico.
Tutti i pazienti dovevano avere malattia misurabile sec. RECIST v.1.1; il tumore primario doveva essere localizzato nell’orofaringe, cavità orale, ipofaringe o laringe; ECOG PS = 0 oppure 1.
Tutti i pazienti arruolati ricevevano:
- Pembrolizumab 200 mg/IV/ogni 3 settimane;
- Carboplatino AUC 5 mg/mq/mm/IV/die 1- cicli ogni 3 settimane;
- Paclitaxel 100 mg/mq/IV/dei 1 e 8 ogni 3 settimane oppure 175 mg/mq/IV/dei 1 ogni 3 settimane.
L’endpoint primario era la RISPOSTA OBIETTIVA valutata secondo i criteri RECIST v 1.1 da parte di una revisione centrale indipendente in cieco (BICR=blinded indipendent central review).
RISULTATI
Tra Ottobre 2020 e Aprile 2022 sono stati scrinati 149 pazienti e 101 sono stati arruolati nello studio e hanno ricevuto almeno una dose di trattamento. Le caratteristiche basali dei pazienti sono riportate nella Tabella 1.
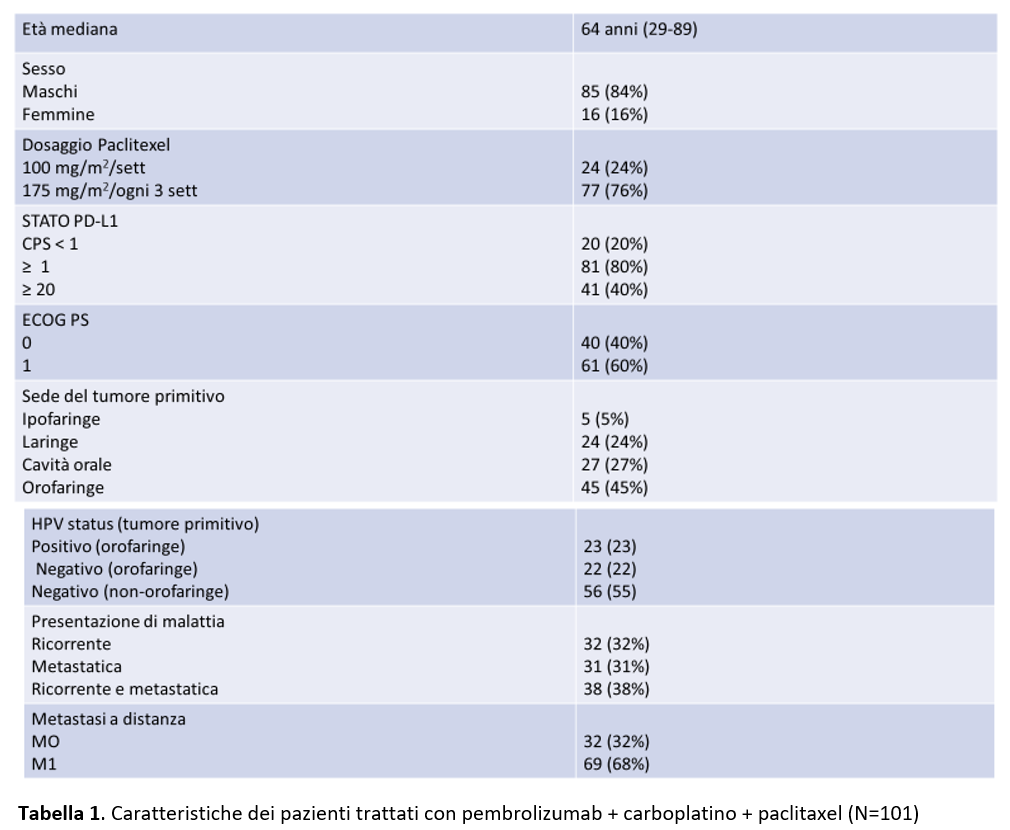
Al tempo del cutoff (20 Febbraio 2023) il follow up mediano era di 18,9 mesi e ancora 15 pazienti (15%) ricevevano trattamento e 86 (85%) avevano interrotto il trattamento nella gran parte dei casi per progressione di malattia (N=62 ; 61%) e per eventi avversi (N=18 ; 18%).
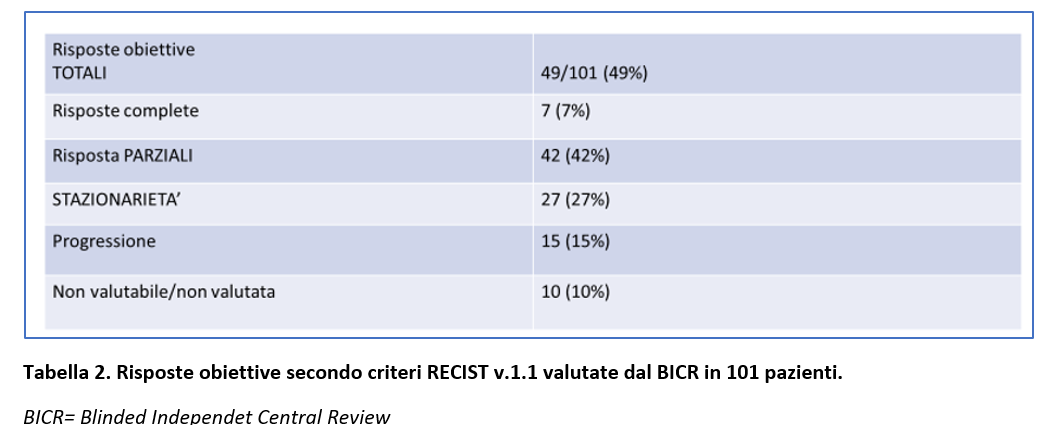
Il tasso di risposte obiettive secondo RECIST v 1.1 valutata dal BICR (Blinded Independet Central Review ) è stato pari al 49% (N=49 ; 95% CI, 38,4-58,7) con 7 (7%) risposte complete e 42 (42%) risposte parziali (Tabella 2).
Il tempo mediano alla risposta (TTR) nei 49 pazienti che hanno avuto una risposta obiettiva confermata è stato di 1,5 mesi (range: 1,1-6,8). La durata mediana della risposta è stata di 5,5 mesi (95% CI ; 4,2-6,7).
Il tasso di controllo di malattia (Stazionarietà+Risposta Parziale+Risposta completa) è stato del 75% (=76 pazienti; 95% CI, 65,7-83,8). I risultati sono stati consistenti in tutti i sottogruppi, con tassi di risposta obiettiva del 65% nel sottogruppo PD-L1 <1, del 65% nel sottogruppo di pazienti con tumore dell’oro-faringe HPV+ e del 50% nel sottogruppo dei pazienti con tumore dell’oro-faringe HPV-negativo.
Alla data del cutoff, 83 pazienti (82%) hanno avuto una progressione di malattia oppure sono deceduti. Il 60% dei pazienti (=61) sono morti.
La PFS mediana è stata pari a 5,6 mesi (95% CI, 5,1-6,7) e il tasso di PFS a 12 mesi è stato del 12% (95% CI, 6,3-20).
La sopravvivenza mediana globale è stata di 13,1 mesi (95% CI, 9,6-15,2) con un tasso di OS a 12 mesi del 52% (95% CI, 42,1-61,5).
TOSSICITA’
Gli eventi avversi correlati al trattamento di qualsiasi grado si sono verificati in 96 pazienti (95%) e i più comuni sono stati: neutropenia (57%), anemia (44%), fatigue (44%) e alopecia (34%).
Eventi avversi di tipo gastro-enterico si sono verificati nel 54% dei pazienti: nausea (28%), diarrea (23%), stipsi (16%) e vomito (15%).
Eventi avversi di grado 3-5 si sono verificati nel 75% dei pazienti:
- Neutropenia 45%
- Anemia 20%
- Leucopenia 17%
- Piastrinopenia 11%
Sono deceduti in totale a causa di eventi avversi 13 pazienti. Eventi avversi da immunoterapia e reazioni infusionali si sono verificati nel 33% dei pazienti.
COMMENTO
I risultati di questo studio a braccio singolo, di fase IV, il KEYNOTE-B10 ha evidenziato una promettente attività antitumorale di pembrolizumab + carboplatino e paclitaxel in prima linea, con un profilo di tossicità maneggevole, nei pazienti con carcinoma squamocellulare ricorrente/metastatico del testa-collo. La risposta antitumorale è risultata essere indipendente da stato di PD-L1, schedula del paclitaxel e presenza/assenza di metastasi a distanza.
Questo schema può essere una alternativa di trattamento in questi pazienti.
Prima dell’inizio dello studio KEYNOTE-B10, erano disponibili pochi dati chimici relativi all’utilizzo di inibitori di PD-1 in combinazione con chemioterapia contenente platino e plaxitaxel nei pazienti con cancro testa-collo e non erano disponibili dati da studi prospettici in prima linea.
Più recentemente, delle review retrospettive di pembrolizumab + platino e taxano hanno concluso che questa combinazione ha attività antitumorale (PATIL V. , 2022; VALADEZ A. , 2020) e un confronto retrospettivo pubblicato nel 2023 come abstract (SUN L. , 2023) in 438 pazienti non ha riportato alcuna differenza in OS mediana tra pembrolizumab + platino e taxano versus pembrolizumab + platino e 5FU.
I risultati dello studio di fase III KEYNOTE-048 che hanno valutato l’efficacia di pembrolizumab + chemioterapia con platino e fluorouracile (n=281) rispetto a cetuximab + chemioterapia (n=300), hanno portato alla approvazione da parte di FDA di pembrolizumab + platino+ fluorouracile come trattamento di prima linea per pazienti con carcinoma squamocellulare di prima linea ricorrente/metastatico dallo stato di PD-L1 (BURTNESS B. 2019).
Ad un follow up di 13 mesi, la OS mediana del gruppo pembrolizumab + platino+ fluorouracile è stata di 13 mesi (95% CI, 10,9-14,7) e la PFS mediana di 4,9 mesi (95% CI, 4,7-6).
Il tasso di risposte obiettive (ORR) è stato del 36% con 6% di risposte Complete, nel tempo mediano alla risposta di 2,1 mesi e una durata mediana della risposta (DOR) di 6,7 mesi.
Nello studio di fase IV KEYNOTE-B10 i risultati sono stati simili:
- ORR del 49% con 7% di risposte complete;
- OS mediana di 13,1 mesi
- PFS mediana di 5,6 mesi.
Sebbene l’endpoint di efficacia dello studio KEYNOTE-B10 basato sulla risposta al trattamento sia stato valutato dal BICR, un limite di questo studio è che non è randomizzato e a braccio singolo senza diretto confronto con altri regimi.
L’eventuale non eleggibilità al cisplatino non è stata valutata in maniera specifica allo screening. Inoltre, l’entità di malattia all’arruolamento può aver influenzato i risultati finali dello studio perché il 68% dei pazienti erano metastatici al basale.
I risultati del KEYNOTE-B10 supportano l’uso di pembrolizumab in combinazione con paclitaxel+ carboplatino come ulteriore opzione di prima linea nei pazienti con carcinoma squamocellulare ricorrente/metastatico, indipendentemente dallo stato di PD-L1 e indipendentemente dalla schedula del paclitaxel.

Bibliografia
Burtness B, Harrington KJ, Greil R, et al: Pembrolizumab alone or with chemotherapy versus cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): A randomised, open-label, phase 3 study. Lancet 394:1915-1928, 2019
Patil V, Alone M, Rai R, et al: Safety and efficacy of pembrolizumab with chemotherapy in locally advanced head and neck cancers. Oral Oncol 127:105824, 2022
Valadez A, Welsh M, Kim C, et al: 201 Carboplatin, paclitaxel and pembrolizumab for the first line treatment of recurrent and/or metastatic head and neck squamous cell carcinoma. Regular Young Invest Award Abstr 8:A216, 2020
Sun L, Cohen RB, Colevas ADD: Platinum/taxane/pembrolizumab vs platinum/5FU/pembrolizumab in patients with recurrent/metastatic (r/m) head and neck squamous cell carcinoma (HNSCC). J Clin Oncol 41, 2023 (16_suppl; abstr 6039)
Link all’abstract:
https://pubmed.ncbi.nlm.nih.gov/39038265/
FREE Full Test- PMC:
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC11361359/


