
EVENT-FREE SURVIVAL BY RESIDUAL CANCER BURDEN WITH PEMBROLIZUMAB IN EARLY-STAGE TRIPLE NEGATIVE BREAST CANCER (TNBC): EXPLORATORY ANALYSIS FROM KEYNOTE-522.
Pusztai L, Denkert C, O’Shaughnessy J, Cortes J, Dent R, McArthur H, Kümmel S, Bergh J, Park YH, Hui R, Harbeck N, Takahashi M, Untch M, Fasching PA, Cardoso F, Zhu Y, Pan W, Tryfonidis K, Schmid P.
Ann Oncol 2024 Feb 17:S0923-7534(24)00046-2. doi: 10.1016/j.annonc.2024.02.002.
Lo studio KEYNOTE- 522 è uno studio Keynote-522 è uno studio randomizzato, placebo-controllato, di fase III che ha valutato efficacia e tossicità del trattamento neo-adiuvante con pembrolizumab-chemioterapia rispetto a placebo-chemioterapia, seguito da pembrolizumab o placebo adiuvante in pazienti con carcinoma mammario triplo negativo STADIO II-III (Figura 1.)

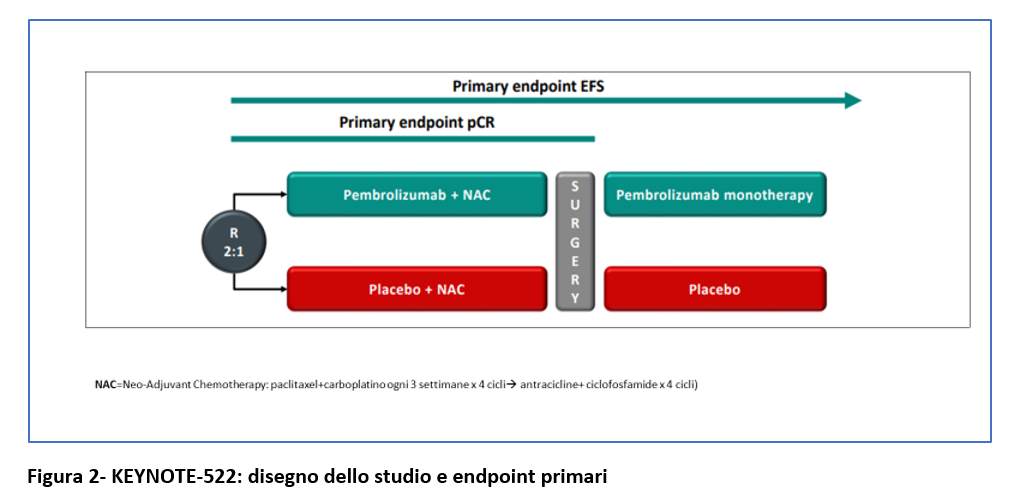
I due endpoint primari dello stadio erano la risposta completa patologica(pCR) e la sopravvivenza libera da eventi (Event-free SURVIVAL- EFS).
La pCR era definita come ypTO/Tis ypNO al momento della chirurgia definitiva.
La EFS era definita come il tempo intercorso tra randomizzazione e progressione di malattia che precludeva la chirurgia definitiva, ripresa locale o a distanza, secondo cancro primitivo o la morte per qualsiasi causa. (Figura 1 e Figura 2).
Da marzo 2017 a settembre 2018 sono stati arruolati 1.174 pazienti, randomizzati (2:1) a pembrolizumab-chemioterapia (=784) e a placebo-chemioterapia (=390).
Nella Tabella 1 sono riportarti i risultati relativi agli endpoint primari.
Residual Cancer Burden (RCB)
Il Residual Cancer Burden (RCB) è stato ideato nel 2007 per fornire un metodo standard per valutare e quantificare l’estensione della malattia residua nella mammella e nei linfonodi ascellari dopo la chemioterapia neoadiuvante (Symmans 2007). Il RCB combina misurazioni delle dimensioni del tumore primario, della proporzione di area tumorale contenente carcinoma invasivo, del numero di linfonodi positivi e della dimensione della metastasi linfonodale maggiore e identifica 4 classi di malattia residua: da RCB-0, corrispondente alla pCR, a RCB-1, RCB-2 e RCB-3 che rappresentano un carico tumorale residuo crescente. Le valutazioni dell’RCB sono risultate altamente riproducibili tra i patologi e le quattro classi sono state convalidate come prognostiche in molti studi (Symmans 2021) e, recentemente, in diversi sottotipi di carcinoma mammario precoce per quanto riguarda l’EFS a 3, 5 e 10 anni in un’analisi congiunta di 5161 pazienti trattate con chemioterapia neoadiuvante tra il 1994 e il 2019 (Yau 2022).
In questa analisi esploratoria prespecificata del KEYNOTE-522, è stata valutata l’Event-Free Surival (EFS) nelle varie categorie di malattia residua al momento della chirurgia valutata secondo l’indice RBC per tutti i pazienti e viene riportata la distribuzione del primo evento per l’EFS per categoria di RCB e gruppo di trattamento.
Nella tabella 2 è riportata la EFS a 36 mesi nelle diverse categorie di malattia residua.

TOSSICITA’
Eventi avversi correlati al trattamento di grado 3 o superiore sono stati osservati nel 76,8% del gruppo Pembrolizumab-chemioterapia e nel 72,2% del gruppo Placebo-chemioterapia Tra questi, sono stati riportati: anemia nel 18,2% del gruppo Pembrolizumab-chemioterapia vs 14,9% del gruppo placebo-chemioterapia e neutropenia (34,6% vs 33,2%).
Tra gli eventi avversi di particolare interesse, sono stati riportati con maggiore frequenza nel gruppo Pembrolizumab-chemioterapia:
-ipotiroidismo (13,7% qualsiasi grado vs 3,3% nel gruppo placebo-chemioterapia);
– ipertiroidismo (4,6% q.si grado vs 1% nel gruppo placebo-chemioterapia);
-reazioni cutanee (4,4% q.si grado vs 1% nel gruppo placebo-chemioterapia);
-insufficienza surrenalica (2,3% q.si grado vs 1,3% nel gruppo placebo-chemioterapia).
CONCLUSIONI
L’aggiunta di pembrolizumab alla chemioterapia ha determinato un minor numero di eventi per la EFS nelle categorie di Residual Cancer Burden RCB-0, RCB-1 e RCB-2, con maggior beneficio nella categoria
RCB-2.
Questi risultati evidenziano che il Pembrolizumab non solo aumenta il tasso di pCR ma anche che aumenta
L’EFS tra la maggior parte dei pazienti che non hanno raggiunto una pCR dopo terapia neoadiuvante con pembrolizumab e chemioterapia.
COMMENTO
Questa analisi esploratoria pre-specificata dello studio KEYNOTE-522 ha evidenziato un beneficio con pembrolizumab in pazienti con carcinoma mammario triplo negativo che hanno ottenuto una pCR (RCB-0) e tra i pazienti con malattia residua RCB-1 e RCB-2. Il beneficio è risultato essere più pronunciato nella categoria RCB-2 , che rappresenta anche la frazione maggiore (55%) di pazienti con malattia residua.
Il piccolo sottogruppo di pazienti della categoria RCB-3 (malattia residua estesa) ha avuto una peggiore prognosi in entrambi i gruppi di trattamento, suggerendo che questa categoria rappresenta un sottogruppo di tumore resistente al trattamento che necessita di ulteriori terapie e ulteriori studi.
Questa analisi esploratoria ha vari limiti:
- sono piccoli i numeri nei vari sottogruppi, specialmente nella categoria RCB-3;
- tutte le analisi sono confronti non randomizzati;
- il disegno dello studio KEYNOTE-522 non permette di distinguere il beneficio derivante dalla somministrazione di pembrolizumab neoadiuvante versus adiuvante.
L’impiego di pembrolizumab nell’ambito del trattamento neoadiuvante del carcinoma mammario triplo negativo (stadi II-III) è autorizzato da EMA e da AIFA (Determina 10 luglio 2023, GU 18/07/2023 Serie Generale n. 166) ed è rimborsato dal Servizio Sanitario Nazionale italiano con la seguente indicazione:
“in associazione a chemioterapia come trattamento neoadiuvante e poi continuato in monoterapia come trattamento adiuvante dopo intervento chirurgico per pazienti con carcinoma mammario triplo negativo localmente avanzato o in fase iniziale ad alto rischio di recidiva (cT1c cN1-N2; cT2-4 cN0-N2)”.
BIBLIOGRAFIA
Schmid P, Cortes J, Pusztai L et al. Pembrolizumab for early triple-negative breast cancer. N Engl J Med 2020; 382: 810-821
Schmid P, Cortes J, Dent R et al. Event-free survival with pembrolizumab in early triplenegative breast cancer. N Engl J Med 2022; 386: 556-567.
Symmans W.F. et al., Measurement of Residual Breast Cancer Burden to Predict Survival After Neoadjuvant Chemotherapy. J Clin Oncol 2007; 25: 4414-4424. FREE ACCESS https://ascopubs.org/doi/10.1200/JCO.2007.10.6823?url_ver=Z39.88-2003&rfr_id=ori:rid:crossref.org&rfr_dat=cr_pub%20%200pubmed
Symmans W.F. et al. Assessment of Residual Cancer Burden and Event-Free Survival in Neoadjuvant Treatment for High-risk Breast Cancer. JAMA Oncol. 2021; 7: 1–10.
Yau C et ak.; I-SPY2 Trial Consortium. Residual cancer burden after neoadjuvant chemotherapy and long-term survival outcomes in breast cancer: a multicentre pooled analysis of 5161 patients. Lancet Oncol., 2022; 23:149-160.
Link all’abstract
https://pubmed.ncbi.nlm.nih.gov/38369015/


